
3. Группа лепидокрокита-гётита
Сюда относятся так называемые моногидраты трехвалентных металлов: Al, Fe, Мn и Со. Эти соединения диморфны; кристаллизуются в ромбической сингонии.
К подгруппе лепидокрокита (FeOOH) относится алюминиевый его аналог-бёмит (АlOОН), а к подгруппе гётита (HFeO2)-диаспор (НАlO2). Здесь же опишем манганит, эмпирическая формула которого аналогична указанным соединениям, но по остальным признакам он имеет мало общего с ними.
Бёмит-АlOОН. Назван по фамилии Бёма, установившего путем рентгенометрических исследований в боксите присутствие этого минерала, сходного по кристаллической структуре с лепидокрокитом (FeOOH).
Химический состав такой же, как диаспора. Аl2O3 84,97% (по формуле). Содержит также SiO2, Fe2O3, повидимому, в виде механической примеси опала и гидроокислов железа, а также Ga2O3.
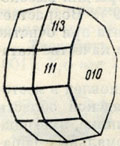
Рис. 199. Кристалл бёмита из Вишневых гор. По Э. М. Бонштедт-Куплетской
Сингония ромбическая. Кристаллическая структура аналогична структуре лепидокрокита и описана ниже. Облик кристаллов. В трещинах и порах среди боксита, а также продуктов разложения нефелина устанавливается в виде очень мелких пластинчатых или чечевицеобразных кристалликов (рис. 199), представленных обычно комбинациями {010}, {111}, {113}, {110} и др. Характерно, что грани {010} являются блестящими, а грани остальных форм матовыми. Обычно же распространен в виде скрытокристал-лической массы (в бокситах).
Цвет. Бесцветный или белый с желтоватым оттенком. Средний показатель преломления для скрытокристаллических разностей равен 1,640-1,645.
Твердость 3,5. Спайность совершенная по {010}. Уд. вес 3,01-3,06. При прокаливании превращается в γ-Аl2O3 (кубическую модификацию кристаллизующуюся в структуре шпинели).
Диагностические признаки. Ввиду ничтожности размеров кристалликов наиболее надежно устанавливается по дебаеграммам. От диаспора отличается меньшим показателем преломления и более низкой твердостью.
П. п. тр. не плавится, белеет и расщепляется по спайности. В стеклянной трубке выделяет воду. В кислотах не растворим.
Происхождение и Месторождения. До последнего времени бёмит был известен лишь в экзогенных месторождениях боксита (см. гидраргиллит). Недавно он был установлен как низкотемпературный гидротермальный минерал в виде мелких кристаллов (рис. 199) в пустотах среди пегматитов щелочных пород в Вишневых горах (Средний Урал) в ассоциации с водяно-прозрачным гидраргиллитом на игольчатых кристаллах цеолита (натролита). Он образовался, повидимому, в результате гидротермального изменения нефелина.
Лепидокрокит - FeOOH. "Лепидос" по-гречески - пластинка, "крокос" - шафран. Синоним: рубиновая слюдка.
Химический состав тождествен составу гётита. Согласно имеющимся анализам, примесей гораздо меньше, чем в гётите. Так же, как и для гётита, существуют разности, содержащие адсорбированную воду (в тонкокристаллических колломорфных массах), носящие название гидролепидокрокита - FeOOH•аg.
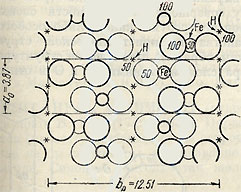
Рис. 200. Кристаллическая структура лепидокрокита - Fe ООН. Крупные кружки - ионы кислорода, малые кружки - ионы Fe3+. Звездочками показаны вероятные положения ионов H1+
Сингония ромбическая. Кристаллическая структура. Как можно видеть на рис. 200, катионы Fe3+ находятся в шестерном окружении ионов кислорода (не показаны лишь передний и задний анионы). Последние располагаются по вершинам искаженных октаэдров, связанных между собой в цепи, вытянутые параллельно оси а. Эти цепи боковыми связями (через ребра октаэдров) друг с другом соединены в непрерывные двойные листы параллельно (010), т. е. перпендикулярно плоскости чертежа (в вертикальном направлении). Как изображено на рис. 200, такие двойные листы соединены друг с другом слабыми водородными связями в виде непрерывных зигзагообразных шнурков: -О-Н-О-Н-О-. Каждый примыкающий к Н-ионам анион О2-, с одной стороны, связан с двумя катионами Fe3+, получая от них по 1/2 валентности, с другой-с двумя Н-катионами, в результате чего имеет место полное насыщение его валентности. Что касается анионов О2-, расположенных внутри двойных листов (см. рис. 200), то их валентность также полностью удовлетворяется долями валентностей, отдаваемых катионами Fe3+ (каждый анион О окружен четырьмя катионами Fe). Таким образом, в строении решетки лепидокрокита принимают участие два типа ионов кислорода, и формулу этого минерала поэтому приходится писать в виде FeOOH. Гидроксильные ионы как таковые отсутствуют в структуре. В структуре же гётита - HFeO2 все кислородные ионы химически эквивалентны. Упаковка ионов в решетке лепидокрокита менее плотная, что сказывается в меньшем его удельном весе. Облик кристаллов. Лепидокрокит встречается в виде пластинчатых по (010) кристалликов в пустотах (рис 201), но чаще в виде тонкочешуйчатых или волокнистых агрегатов. Наблюдались и почковидные агрегаты на стенках жеод.
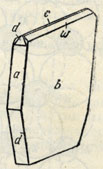
Рис. 201. Кристалл лепидокрокита а {100}, b {010}, с {001}, d {201}, w {031} и t {131}
Цвет лепидокрокита тёмнокрасный до красновато-черного; иногда с золотистым оттенком (в чешуйчатых массах). Черта оранжевая или кирпичнокрасная. Блеск алмазный. В тонких шлифах прозрачен. Ng = 2,51, Nm=2,20 и Np =1,94.
Твердость 4. Спайность весьма совершенная по {010] и совершенная по {001}. Уд. вес 4,09-4,10.
Диагностические признаки. Часто ошибочно принимают за гематит, особенно в плотных агрегатах. Отдельные пластинки лепидокрокита легко узнаются по форме кристалликов, просвечиваемости их красным цветом, оранжево-красной или красной черте и малому удельному весу (отличие от гематита).
П. п. тр. не плавится; при высоких температурах становится черным, магнитным. В стеклянной трубке выделяет воду. В НСl растворяется.
Происхождение и месторождения. Лепидокрокит в виде пластинчатых кристалликов (рубиновой слюдки) иногда наблюдается как один из наиболее поздних минералов гидротермальных месторождений, например в Зигене в Вестфалии (Германия), в жильных железорудных месторождениях Ангаро-Илимского района (в пустотах тонких кварцевых прожилков) и в других случаях. Гораздо чаще он наблюдается в виде концентрических слоев чешуйчатых агрегатов в натечных бурых железняках или на стенках жеод поверхностного происхождения: в Полетаевских месторождениях (к юго-западу от г. Челябинска), в окрестностях г. Липецка и в других местах.
Как по данным микроскопических исследований, так и по данным рентгенометрического изучения продуктов, образующихся при систематическом нагревании, оказывается, что лепидокрокит способен переходить в гётит. Условия, при которых происходят эти превращения, а также условия образования в природе различных модификаций моногидрата окиси железа еще не изучены. Вероятно, здесь играет роль степень кислотности среды (рН), при которой происходит образование гидратов окиси железа.
Диаспор - НАlO2. "Диаспор" по-гречески - рассеяние (некоторые образцы при нагревании, растрескиваясь, распадаются на мелкие частички). Впервые установлен еще в прошлом столетии на Урале.
Химический состав. Аl2O3 85%, Н2O 15%. Известны разности, содержащие в виде изоморфной примеси Fe2O3 (до 7%), Мn2O3 (мангандиаспор), Сr2O3 (до 5%) и SiO2 (до 4%). Устанавливается также повышенное содержание Ga2O3 (до нескольких сотых процента).
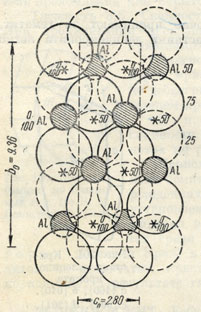
Рис. 202. Кристаллическая структура диаспора. Звездочками показаны вероятные места положения протонов
Сингония ромбическая; ромбо-дипирамидальный в. с. 3L23PC. Кристаллическая структура изображена на рис. 202. Она характеризуется плотной гексагональной упаковкой ионов О2-, причем ионы Аl3+ размещаются в октаэдрических пустотах, т. е. между шестью ионами О. Каждый ион кислорода связан с тремя ионами Аl, т. е. координационные числа для Аl и О те же, что и в кристаллической решетке рутила (6 и 3). Протоны Н1+ располагаются, вероятно, между парами ионов кислорода (рис. 202) и в силу совершенной ничтожности своих размеров не требуют какого-либо особого пространства в кристаллической структуре. Таким образом, практически структура диаспора сложена ионами Аl и О в отношении 1 : 2 (как в рутиле). Сходство с рутилом, как показал Н. В. Белов, заключается и в самих структурах этих минералов, с той разницей, что в диаспоре (гётите), вместо одинарных колонок в рутиле, вдоль оси с тянутся сдвоенные колонки плотнейшей упаковки. Этим объясняются столбчатый облик кристаллов, спайность и коленчатые двойники с углом около 122°.
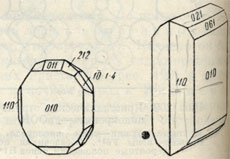
Рис. 203. Кристаллы диаспора
Облик кристаллов. Встречающиеся кристаллы имеют тонкопластинчатые, иногда таблитчатые по {010} формы (рис. 203), нередко столбчатые по оси с. Наблюдается вертикальная штриховатость граней. Обычно распространен в листоватых или тонкочешуйчатых агрегатах.
Цвет диаспора желтовато-бурый, белый, светлофиолетовый, зеленовато-серый. Блеск стеклянный, на плоскостях спайности перламутровый. Черта белая. Ng=l,750, Nm=1,722 и Np=1,702.
Твердость 6-7. Очень хрупкий. Спайность по {010} средняя. Уд. вес 3,3-3,5. При прокаливании переходит в α-Аl2O3 (корунд).
Диагностические признаки. Для диаспора характерны листоватые агрегаты, высокая твердость (отличие от гидраргиллита, слюд и др.). Смешать можно только с некоторыми почти не различимыми по внешним признакам разностями хлоритоида (алюмосиликата Fe и Аl), встречающегося иногда совместно с ним и корундом в метаморфических породах. В отличие от него, диаспор не разлагается в H2SO4 и, кроме того, отличается по некоторым оптическим свойствам.
П. п. тр. не плавится. В кислотах и КОН не растворяется. В H2SO4 разлагается лишь после сильного прокаливания. В пробирке при накаливании, распадается на мелкие белые чешуйки.
Происхождение. Изредка встречается в некоторых контактовометасоматических и гидротермальных месторождениях среди мраморизованных известняков в ассоциации с корундом, мусковитом, гематитом, рутилом и др.
В больших массах в виде тонкочешуйчатых агрегатов распространен в экзогенных месторождениях бокситов в парагенезисе с гидраргиллитом, бёмитом и др.
Часто встречается в метаморфических породах, совместно с корундом, хлоритоидом и другими минералами (в месторождениях наждака, вероятно, как продукт метаморфизма бокситов), иногда в кристаллических сланцах как породообразующий минерал в сопровождении дистена.
Месторождения. О практическом значении бокситов см. выше (гидраргиллит). В ассоциации с корундом и алюмосиликатами встречается в месторождениях наждака на Урале: Косой Брод (Свердловский район) в мраморированных известняках, по р. Борзовке (Кыштымский район), в месторождении Акташ (Узбекская ССР) в ассоциации с дюмортьеритом, пирофиллитом, алунитом и корундом, а также в других местах.
В крупных пластинках и кристаллах распространен в наждачных копях Честер в Массачузетсе (США), на о. Наксос (Греция).
Гётит - HFeO2 и Лимонит(гидрогётит) - HFeO2•aq. Гётит назван в честь поэта В. Гёте (1749-1832). Первоначально этот минерал был назван онегитом (по месту нахождения на острове в Онежском озере), но так как его свойства не были описаны, это название не привилось в минералогической литературе. Синоним: "игольчатая железная руда" (в немецкой литературе).
Название лимонит происходит от греческого слова "лемон" - луг (имелись в виду луговые и болотные руды гидроокислов железа).
Химический состав. Fe2O3 89,9%, Н2O 10,1%. Содержание воды часто бывает выше, чем полагается по формуле: до 12-14% (лимонит). В связи с этим раньше выделяли несколько минеральных видов, отличающихся друг от друга по содержанию воды и некоторым физическим свойствам. Рентгенометрически установлено, что в действительности существует одно соединение с отношением Fe2O3 : Н2O=1 : 1, обладающее определенной кристаллической решеткой. Все более богатые водой разности гидроокислов железа по существу являются гидрогелями и содержат адсорбированную воду в разных количествах (в зависимости от степени дегидратации).
Так называемый турьит по рентгенометрическим и термическим исследованиям оказался смесью гётита с гидрогематитом и не принадлежит к числу самостоятельных минералов.
Скопления природных гидроокислов железа в своей массе, как правило, представляют собой смеси гётита с лимонитом, а также гидроокислами кремнезема, глинистым веществом и др. Такие смеси обычно называются бурыми железняками.

Рис. 204. Кристалл гетита
Сингония ромбическая; ромбодипирамидальный в. с. Кристаллическая структура аналогична структуре диаспора. Облик кристаллов и агрегаты. Редко встречающиеся кристаллы имеют игольчатый или столбчатый облик (рис. 204). Обычно наблюдается в натечных, почковидных или сталактитовых формах (рис. 44) с тонким радиально- или параллельноволокнистым строением в изломе ("игольчатая железная руда") или в сплошных плотных, пористых ноздреватых, шлаковидных, порошковатых массах. Распространены псевдоморфозы по кристаллам пирита и другим сульфидам железа. Встречается также в виде оолитов, бобовин, конкреций и жеод.
Цвет лимонита и гётита темнобурый до черного. Порошковатый или охристый лимонит, нередко образующийся при физическом выветривании за счет плотного черного лимонита и силикатов железа, обладает довольно светлым желто-бурым цветом. Как показали сравнительные химические и рентгенометрические исследования, эта охристая разность ничем особенным не отличается от плотного лимонита. Черта гётита бурая с красноватым оттенком. Лимонит большей частью имеет светлобурую или желто-бурую черту. Блеск гётита алмазный до полуметаллического. На поверхности почковидных или сталактитовых масс лимонита часто обнаруживается гётит в виде блестящих смоляно-черных тонких корочек. Nm = 2,35-2,39.
Твердость гётита 4,5-5,5, лимонита 4-1 (в зависимости от физического состояния). Спайность гётита по {010} совершенная. Уд. вес гётита 4,0-4,4, у лимонита колеблется от 3,3 до 4,0.
Диагностические признаки. Гётит и лимонит сравнительно легко узнаются по колломорфным образованиям, бурой черте и желто-бурым охристым примазкам.
П. п. тр. плавятся; при продолжительном нагревании становятся сильно магнитными. В стеклянной трубке выделяют воду, краснеют, превращаясь в безводную Fe2O3. В НСl медленно растворяются.
Происхождение. Гётит в виде игольчатых или столбчатых кристалликов крайне редко наблюдается как эндогенный минерал: в пустотах мелафиров, в аметистовых жеодах на Волк-Острове (Онежское озеро); иногда в гидротермальных месторождениях как один из наиболее низкотемпературных минералов в пустотах, например в Пршибраме (Чехословакия), в ассоциации с более ранними, не затронутыми выветриванием сфалеритом и пиритом.
В главной же массе гётит и лимонит распространены как экзогенные минералы, и притом почти исключительно в виде колломорфных или метаколлоидных масс. Они образуются преимущественно в результате гидролиза солей, возникающих при окислении и разложении железосодержащих минералов: сульфидов, карбонатов, силикатов и других, в которых железо присутствует в двухвалентной форме. Образование гидроокислов железа на поверхности мы наблюдаем буквально всюду и притом в самых различных видах.
В значительных массах бурые железняки образуются в зонах окисления сульфидных месторождений. Это так называемые железные шляпы, представленные рыхлыми, комковатыми и плотными массами, состоящими главным образом из лимонита, гётита, иногда лепидокрокита и др.
Большие массы гидроокислов железа заключены в осадочных месторождениях бурых железняков молодого (третичного) возраста, образовавшихся в морских и озерных бассейнах. Накопление осадков гидроокислов железа, так же как и других гидроокислов, в прибрежных зонах этих бассейнов, очевидно, происходит путем коагуляции приносимых поверхностными водами коллоидных растворов в морских водах под действием электролитов, а в пресных озерах - в результате, вероятно, жизнедеятельности ферробактерий. Правда, в ряде осадочных месторождений гидроокислы железа, кроме того, дополнительно образуются в результате современного окисления попавших в зону окисления фаций карбонатных и силикатных руд железа.
Таким образом, лимонит и гётит почти исключительно образуются на самой поверхности, в условиях полного доступа кислорода и влаги.
При региональном метаморфизме гидраты железа обезвоживаются и превращаются в безводные окислы (гематит и магнетит).
Практическое значение. Бурые железняки, так же как и гематитовые и магнетитовые руды, являются важнейшим сырьем для выплавки чугунов и сталей в доменных печах. В процессе нагревания этих руд в печах происходят полное их обезвоживание и образование чрезвычайно тонкопористых масс.Так как скорость восстановления руд сильно зависит от удельной поверхности массы, то эти руды являются более экономичными по сравнению с магнетитовыми и гематитовыми рудами. Поэтому требования к минимальному содержанию железа в них снижаются до 35-40% (вместо 50-60% для плотных магнетитовых и гематитовых руд).
Месторождения. Из весьма многочисленных и разнообразных в генетическом отношении месторождений бурых железняков мы укажем лишь некоторые наиболее главные.
В пределах СССР крупное месторождение преимущественно крупнооолитовых бурых железняков находится на Керченском полуострове. Мощный рудный пласт залегает в мульдах среди осадков третичного возраста. Эти руды содержат 34-42% Fe и обогащены фосфором. Известное Бакальское месторождение бурых железняков (Ю. Урал, к юго-западу от г. Златоуста) образовалось в виде крупных железных шляп в результате окисления кристаллических сидеритовых руд, невидимому гидротермального происхождения. Наряду с мягкими рыхлыми рудами широко распространены жеоды бурых железняков, часто очень крупные. Стенки полостей покрыты натеками лимонита и гётита. Эти руды малофосфористые, высокого качества. Халиловское месторождение бурых железняков (у ж.-д. ст. Халилово, Чкаловской области, Ю. Урал) образовалось в юрское время за счет выветривания и размыва массивов ультраосновных (серпентинитовых) пород. Поэтому бурые железняки несколько обогащены такими элементами, как никель и хром, являющимися ценными легирующими компонентами сталей. Никеленосные бурые железняки как остаточные продукты выветривания серпентинитов широко распространены на Урале; назовем Елизаветинское месторождение около г. Свердловска.
Манганит - Мn••Мn••••O2[ОН]2, или МNO2 - Мn[ОН]2. Наличие двух-и четырехвалентного (а не трехвалентного) марганца установлено путем изучения магнитной анизотропии ионов.
Химический состав. МnО 40,4%, МNO2 49,4%, Н2O 10,2%. Примеси: SiO2 (до нескольких процентов), Fe2O3 (до 1%), в незначительных количествах Аl2O3, СаО и др. Содержание Н2O в скрытокристаллических и оолитовых манганитовых массах, так же как и в гётите, бывает больше, чем это полагается по формуле (гидроманганит). Избыточная часть воды является адсорбированной, как это устанавливается по кривым обезвоживания.
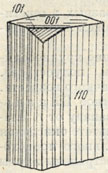
Рис. 205. Кристалл манганита
Сингония моноклинная. Кристаллическая структура существенно отличается от структуры гётита и пока еще не расшифрована. Облик кристаллов призматический (рис. 205), столбчатый по оси с. Грани {110} сильно исштрихованы в вертикальном направлении. Агрегаты. В пустотах гидротермальных месторождений нередко встречается в виде друз столбчатых кристаллов. В осадочных месторождениях широко распространены тонкокристаллические агрегаты. Наблюдается также в виде оолитов, изредка в натечных формах.
Цвет манганита черный. Черта бурая. Блеск полуметаллический. Ng=2,53, Nm=2,24 и Np=2,24.
Твердость 3-4. Хрупок. Спайность по {010} совершенная. Уд. вес 4,2-4,33.
Диагностические признаки. Кристаллы легко узнаются по столбчатому облику, характерной штриховке граней призмы и по бурой черте. Для колломорфных богатых водой разностей характерен бурый цвет самого минерала и черты. Для точной диагностики необходимы рентгенограммы.
П. п. тр. не плавится. В закрытой стеклянной трубке обильно выделяет воду. Перл буры и фосфорной соли в окислительном пламени фиолетовый (присутствие марганца). В концентрированной НСl растворяется с выделением хлора.
Происхождение. Вообще образуется при недостатке кислорода. Встречается в виде друз кристаллов в некоторых гидротермальных месторождениях марганца как один из последних по времени выделения минералов в парагенезисе с баритом и кальцитом.
В больших массах встречается в осадочных месторождениях в виде оолитов и сплошных масс, занимая промежуточное положение между фациями псиломелано-пиролюзитовых руд (соединений четырехвалентного марганца) и карбонатных руд, содержащих двухвалентный марганец.
В глинах обнаруживается иногда в виде желваков с радиальнолучистым строением.
В зоне окисления не устойчив. Легко превращается в скрытокристаллический, почти безводный МNO2, т. е. весь марганец окисляется до четырехвалентного состояния. Поэтому в марганцевых шляпах манганит почти не встречается.
Практическое значение. Наряду с пиролюзито-псиломелановыми рудами представляет собой важное сырье для ферромарганца и других сплавов с железом (шпигеля, силикошпигеля), употребляемых при выплавке сталей.
Месторождения. В значительных массах манганит известен в Чиатурском месторождении в виде оолитовых руд бурого цвета. В шарообразных конкрециях черного цвета широко распространен также в Никопольском месторождении (Украина).
Манганит в виде кристаллов, нередко крупных, известен в гидротермальном месторождении Ильфельд в Гарце, Ильменау в Тюрингии (Германия) и в других местах.
|
ПОИСК:
|
© IZNEDR.RU, 2008-2020
При использовании материалов сайта активная ссылка обязательна:
http://iznedr.ru/ 'Из недр Земли'
При использовании материалов сайта активная ссылка обязательна:
http://iznedr.ru/ 'Из недр Земли'