
11. Группа кварца
Минералы, входящие в эту группу, имеют один и тот же очень простой состав - SiO2. Они представляют собой ряд полиморфных модификаций.
Эти минералы по кристаллическому строению занимают совершенно особое положение среди окислов. Как мы потом увидим, кристаллические структуры их имеют прямое отношение к силикатам. На этом основании некоторые авторы эту группу минералов рассматривают в разделе силикатов. Но так как кварц по своей химической природе является типичным окислом, то мы, согласно принятой нами установке, должны его рассматривать в этом разделе.
Из относящихся сюда полиморфных модификации SiO2 три главные формы имеют самостоятельные названия: кварц, тридимит и кристобалит. Их модификации принято обозначать с приставками греческих букв α и β*.
*(Некоторые авторы, в частности П.Ниггли, Ф.Ринне, А.Е.Ферсман и другие, придерживаются обратного обозначения более низкотемпературную модификацию α-кварц они обозначают как β-кварц, α-кристобалит-β-кристобалит и т.д.)
В природе существует также гидратированный кремнезем - опал SiO2•nH2O, который мы рассмотрим особо.
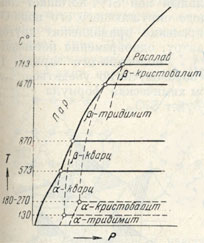
Рис. 180. Однокомпонентная система - SiО2. Кривые упругости паров различных модификации SiO2 показаны схематически. Для каждой данной температуры более устойчива та модификация, для которой упругость пара меньше (т. е. кривая ближе к оси ординат)
Общая картина полиморфных превращений SiO2 изображена на рис. 180 в виде диаграммы состояния ТР. Установлен следующий ряд энантиотропных превращений:
α-кварц⇔β-кварц⇔β-тридимит⇔β-кристобалит⇔расплав. 573° 870° 1470° 1713°
Кроме того, для тридимита и кристобалита в области низких температур в сильно переохлажденном состоянии известны также энантиотропные превращения:
α-тридимит⇔β-тридимит и α-кристобалит⇔β-кристобалит. 130° 180-270°
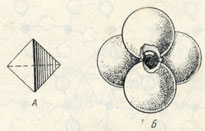
Рис. 181. А - тетраэдр, поставленный на ребро; вершины его являются центрами ионов кислорода в тетраэдрической группе SiО4 (Б), внутри которой располагается ион Si4+. Масштаб для А и В один и тот же
Кристаллическая структура кварца, как и других полиморфных модификаций, характеризуется той особенностью, что ион Si4+ всегда находится в четверном окружении ионов O2- (рис. 181), расположенных по вершинам тетраэдра. Каждая вершина такого тетраэдра одновременно служит вершиной другого смежного тетраэдра (рис. 182). Таким образом, кристаллические решетки этих минералов состоят как бы из каркасов сцепленных друг с другом тетраэдров. Способ сцепления во всех модификациях один и тот же (через вершины тетраэдров), но ориентировка и общая симметрия в расположении их различны. В целом упаковка ионов кислорода не плотная: в каркасах имеются "пустотки" между тетраэдрами. В низкотемпературных модификациях они обладают малыми размерами, а в высокотемпературных, более "рыхло" построенных модификациях они крупнее. В прямой зависимости от этого находятся и удельные веса, а также показатели преломления.
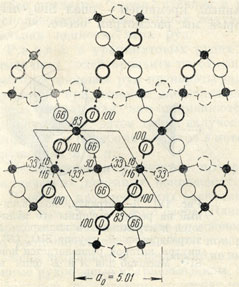
Рис. 182. Кристаллическая решетка более высокотемпературной модификации β-кварца в проекции на плоскость (0001). Цифры означают относительные высоты ионов над плоскостью чертежа
Так как каждый ион кислорода является общим для двух смежных тетраэдров SiO4, то он всюду располагается между двумя ионами кремния, тогда как каждый ион Si4+ находится в четверной координации ионов кислорода. Отсюда и координационные числа 2 и 4. При рассмотрении тетраэдров SiO4 легко видеть, что каждый положительный ион Si4+ погашает лишь половину отрицательной валентности каждого окружающего его иона О2-, но так как каждый ион кислорода одновременно принадлежит другому тетраэдру, одновременно погашается и вторая половина его заряда. Таким образом, легко убедиться, что в целом химическая формула соединения будет SiО2.
α-кварц-SiO2. Эту устойчивую при низких температурах модификацию обычно называют просто кварцем; происхождение названия остается неизвестным. Кварц является одним из наиболее распространенных в земной коре и наилучше изученных минералов.
Химический состав. Теоретическому составу, очевидно, отвечают бесцветные прозрачные разновидности. Разности, окрашенные в молочно-белый цвет, в виде механических примесей в разных количествах могут содержать газообразные, жидкие и твердые вещества: СO2, Н2O, углеводороды, NaCl, СаСO3, в ряде случаев включения мельчайших кристалликов рутила, актинолита и других минералов.
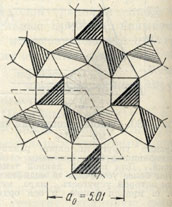
Рис. 183. Та же кристаллическая решетка, что и на рис. 182, но и изображении в виде тетраэдров SiО4. Линиями различной степени жирности (на затененной стороне тетраэдров) показано относительное положение этих тетраэдров над плоскостью чертежа. Легко видеть, что тетраэдры, примыкающие к внутреннему шестиугольнику, расположены по винтовой оси шестого порядка (по двухходовому винту)
Сингония. Более высокотемпературная модификация β-кварц кристаллизуется в гексагональной сингонии, гексагонально-трапецоэдрическом в. с. L66L2. Более устойчивая при температурах ниже 573° (при атмосферном давлении) модификация α-кварц кристаллизуется в тригональной сингонии, тригонально-трапецоэдрическом в. с. L33L2 Кристаллические структуры довольно просты в структурной схеме. На рис. 182 и 183 в одинаковом масштабе изображена Кристаллическая структура β-кварца в проекции вдоль оси с на плоскость (0001). В каждом тетраэдре SiO4 два кислородных иона располагаются несколько выше, а другие два-несколько ниже, чем ион кремния. Группы тетраэдров лежат в трех слоях на различных высотах их относительное положение над плоскостью чертежа показано линиями разной жирности и цифрами при кружках (рис. 182). Как можно заметить на рис. 183, тетраэдры образуют спирали, каждая из которых закручивается в одну и ту же сторону. Так называемые правые и левые кварцы тем и отличаются, что заворот этих спиралей происходит в правую или в левую сторону. Поворот вокруг шестерной оси на 60° и перенос на одну треть высоты элементарной ячейки вдоль оси с приводит к совпадению с прежней позицией тетраэдров (рис. 183).
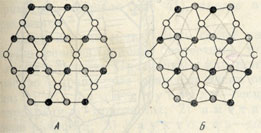
рис. 184. Соотношения в кристаллических структурах β-кварца (A) и α-кварца (Б) Показаны только ионы кремния, высотное положение которых отмечено различной степенью затененности кружков
Низкотемпературная модификация α-кварц по своей кристаллической структуре лишь несколько отличается от β-кварца. На рис. 184 изображены их соотношения в проекции на плоскость (0001), причем показаны лишь ионы кремния. Как видим, при полиморфном превращении высокотемпературной модификации в низкотемпературную происходят небольшие смещения центров кремнекислородных тетраэдров, в результате чего имеет место уплотнение решетки и понижение ее симметрии: шестерные оси превращаются в тройные. При этом тип связи между тетраэдрическими группами не меняется. В процессе превращения не происходит изменений в направлениях заворота спиралей (в правую или левую сторону).
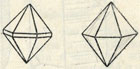
Рис. 185. Кристаллы β-кварца. Гексагональная пирамида (справа) в комбинации с гексагональной призмой (слева)
Облик кристаллов. Кристаллы β-кварца, вернее параморфозы α-кварца по нему, встречающиеся в богатых кремнеземом эффузивных породах (липаритах, кварцевых порфирах и др.) как ранние выделения из жидкой магмы, имеют облик гексагональной дипирамиды, причем грани призмы сильно укорочены или отсутствуют вовсе (рис. 185). Они обычно очень мелки, но в некоторых породах достигают 1-2 см в поперечнике. Низкотемпературный α-кварц в хорошо образованных кристаллах встречается только в пустотах или рыхлых средах. Известны отдельные кристаллы очень крупных размеров, до 1 и даже 40 т весом. Формы кристаллов хотя и весьма разнообразны, по чрезвычайно характерны по присутствию граней призмы m [1010], часто с горизонтальной штриховкой, граней ромбоэдров r [1011] и z [0111], тригональной дипирамиды s {1121}, тригонального трапецоэдра х [5161] и др. (рис. 186). Встречаются индивиды, в которых грани главных ромбоэдров одинаково развиты, и кристаллы в таких случаях принимают облик "гексагональной дипирамиды". Однако ромбоэдры всегда отличаются друг от друга по физическим признакам: грани одного блестяши, другого - матовы, фигуры травления также не одинаковы. По положению граней тригонального трапецоэдра {5161} и дипирамиды {1121} различают правый и левый кварц (рис. 186). Эти грани приурочены к ребрам призмы (через 120е), располагаясь вверху и внизу, но по разные стороны ребра.
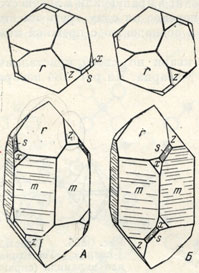
Рис. 186. Левый (А) и правый (Б) кварц m {1010}, r {1011}, z {0111}, s{1121}, х {5161}
Кроме явнокристаллических модификаций α- и β-кварца известны скрытокристаллические разности, обладающие волокнистым строением: халцедон и кварцин, отличимые друг от друга только по оптическим свойствам (в частности, по оптическому знаку).
Двойники наблюдаются весьма часто и по разным законам.
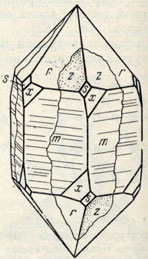
Рис. 187. Дофинейский двойник (схема) Границы между двумя индивидами заметны по сутурной линии
1) Дофинейские двойники (рис. 187) столь совершенно прорастают друг друга, что похожи на простые кристаллы, от которых они отличаются тем, что грани трапецоэдра х наблюдаются в удвоенном количестве (рис. 188) и выводятся друг из друга поворотом вокруг вертикальной оси не на 120°, а на 60°. Грани призмы обоих индивидов сливаются, а грани ромбоэдра r совпадают с гранями ромбоэдра z (рис. 187). Оптические оси обоих индивидов параллельны, и потому двойниковое строение можно установить только путем травления (рис. 189-А). Двойниковые швы извилистые
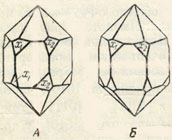
Рис. 188. Дофинейский (А) и бразильский (Б) двойники (схема)
2) Бразильские двойники (рис. 188) отличаются от дофинейских тем, что в них грани трапецоэдров, наблюдающиеся в двойном количестве, выводятся иначе: отражением в вертикальной плоскости. Двойниковое строение легко обнаруживается в поляризованном свете и путем травления (см. рис. 189-Б). В отличие от строения дофинейских двойников, здесь мы наблюдаем прямолинейные двойниковые швы.
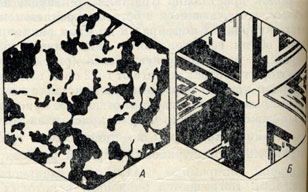
Рис. 189. Протравленные сечения кристаллов кварца (перпендикулярно оптической оси). А- дофинейский двойник, границы индивидов очень неправильные, Б - бразильский двойник с прямыми границами двойниковых индивидов
3) Японские двойники по тригональной дипирамиде {1122}; индивиды наклонены друг к другу под углом 84°34'.
Агрегаты. В пустотах широко распространены друзы кристаллов кварца (рис. 40), иногда в срастании с кристаллами других минералов. Сплошные же массы кварца представляют зернистые агрегаты. Строение плотных агрегатов легко устанавливается в тонких шлифах под микроскопом при скрещенных николях. Халцедон, обладающий скрытоволокнистым строением, часто наблюдается в виде корок, натечных почковидных форм или сферолитов, но чаще в виде желваков, носящих название кремней. Агаты (кремнистые жеоды) имеют концентрически-зональное строение, обусловленное перемежаемостью различно окрашенных слоев халцедона, иногда кварца. Центральные части жеод нередко сложены кристаллически-зернистым кварцем (рис. 41), иногда в виде щеток кристаллов.
Цвет кварца может быть самый различный, но обычно распространены бесцветные, молочно-белые и серые окраски. Прозрачные или полупрозрачные красиво окрашенные разности носят особые названия:
- горный хрусталь - бесцветные водянопрозрачные кристаллы;
- аметист - фиолетовые разности;
- раухтопаз - дымчатые прозрачные разности, окрашенные в сероватые или буроватые тона;
- морион - кристаллы кварца, окрашенные в черный цвет;
- цитрин - золотисто-желтые или лимонно-желтые кристаллы.
Кроме перечисленных прозрачных разностей кварца, наблюдаются явно аллохроматически окрашенные кристаллы кварца благодаря включениям посторонних минералов, также имеющие свои названия:
- празем - зеленоватый кварц с включениями иголочек зеленого актинолита;
- авантюрин - желтоватый или буровато-красный кварц с мерцающим отливом, обусловленным мельчайшими включениями слюды, железной слюдки (Fe2O3) и др.
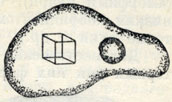
Рис. 190. Газовый пузырек и кристаллик галита в капельке жидкости, включенной в кварц
Широко распространенный в гидротермальных месторождениях молочно-белый цвет кварцевых масс в одних случаях обязан содержанию в них большого количества микроскопических жидкостей и газов. Почти всегда в жидких включениях наблюдается подвижной пузырек газа, по которому легко узнается жидкость, а иногда даже кристаллики NaCl (рис. 190). При нагревании при определенной температуре эти кристаллики растворяются, затем исчезают пузырьки газа и образуется однородная жидкая фаза. При охлаждении она вновь становится неоднородной. Таким путем можно примерно установить, при какой температуре мог произойти захват этих жидких фаз в процессе кристаллизации кварца. В других случаях молочно-белый цвет кристаллов кварца обусловлен сильной трещиноватостью, возникшей при динамических воздействиях (подобно тому, как совершенно прозрачный лед при ударе молотком в поврежденном месте становится молочно-белым).
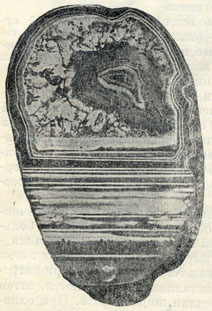
Рис. 191. Агат частью с горизонтальными, частью с концентрическими различно окрашенными слоями
Халцедон чаще, чем кристаллический кварц, бывает окрашен в самые различные цвета и оттенки: молочно-серый, синевато-черный (сапфирин), желтый, красный, оранжевый (сердолик), коричневый, бурый (сардер), зеленый (плазма), яблочно-зеленый от соединений никеля (хризопраз), зеленый с красными пятнышками (гелиотроп) и др. Агаты или ониксы сложены часто тончайшими различно окрашенными концентрически-зональными или плоскопараллельными слоями халцедона (рис. 191), могут иметь самые различные сочетания оттенков: черного с белым (арабский оникс), бурого с белым (сардоникс), красного с белым (карнеолоникс) и др.
Блеск кварца стеклянный, халцедона-восковой до матового. Оптические константы. Кварц оптически одноосный, положительный. Ng = 1,553 и Nm = 1,544. Он обладает способностью вращать плоскость поляризации в ту или другую сторону в зависимости от того, имеем ли мы дело с правым или с левым кварцем.
Твердость 7. Спайность отсутствует или весьма несовершенная по ромбоэдру. Излом раковистый. Уд. вес 2,5-2,8, для чистых разностей 2,65; B-кварц, обладающий менее плотной решеткой, имеет несколько меньший удельный вес. Прочие свойства. Кварц способен пропускать ультрафиолетовые лучи. Обладает свойством пьезоэлектризации: под влиянием механических напряжений в нем возникают электрические заряды. Электрическими осями являются двойные, причем тот конец каждой двойной оси, который упирается в ребро, срезанное гранями трапецоэдра, электризуется отрицательно, а противоположный конец-положительно. Температура плавления кварца 1713°. При застывании расплава легко образуется кварцевое стекло (аморфный кварц), обладающее рядом особых свсйств (кислотоупорностью, низким коэфициентом расширения, способностью пропускать ультрафиолетовые лучи и др.).
Диагностические признаки. Кристаллы кварца легко узнаются по характерным для них формам. Кварц в плотных агрегатах устанавливается по высокой твердости, раковистому излому и отсутствию спайности.
Халцедон от похожих на него минералов (опала, смитсонита - ZnCO3, скрытокристаллического флюорита и других) отличается главным образом по твердости. Легко отличим также по оптическим свойствам.
П. п. тр. не плавится. С кислотами не реагирует, за исключением HF, с которой легко образует летучее соединение - SiF4. Поддается влиянию щелочей. На халцедон сильно действует КОН.
Происхождение. Кварц, будучи широко распространен в природе, входит в состав самых различных по генезису горных пород и рудных месторождений.
Во многих интрузивных и эффузивных кислых изверженных породах он, так же как полевые шпаты и слюды, является существенной составной частью (в гранитах, гнейсах, кварцевых порфирах и др.). Порфировые кристаллы кварца в кислых эффузивных породах обладают кристаллически-зональным строением, часто содержат включения вулканического стекла.
В крупных кристаллах (раухтопаз, морион, аметист и др.) он встречается в пустотах среди пегматитов также в ассоциации с полевыми шпатами, мусковитом, иногда топазом, бериллом, турмалином и другими минералами. Часто наблюдаются закономерные срастания его с крупными индивидами калиевых полевых шпатов-ортоклаза или микроклина, напоминающие в приполированных штуфах еврейские письмена. Характерно, что все эти включения кварца в каждом данном кристалле полевого шпата оптически ориентированы одинаково.
Как постоянный жильный минерал, и притом в значительных массах, кварц распространен в чрезвычайно многочисленных на земном шаре гидротермальных месторождениях в ассоциации с самыми различными минералами: касситеритом, вольфрамитом, золотом, молибденитом, пиритом, халькопиритом, турмалином, кальцитом, хлоритами и др. Почти всегда кварц содержит микроскопические включения газов, жидкостей и твердых минеральных веществ.
Агаты и ониксы в виде миндалин (секреций) самых различных форм и размеров широко распространены во многих эффузивных горных породах - мелафирах, базальтах, андезитах и др. (измененных пузыристых лавах). Образование их связано с циркуляцией концентрированных коллоидных растворов кремнезема в последний, заключительный этап гидротермальной деятельности.
При экзогенных процессах кварц и халцедон в виде тонкозернистых агрегатов образуются при дегидратации и раскристаллизации гелей кремнезема. При этом известны случаи образования в пустотах кристаллов кварца, например в трещинах среди окремненных при поверхностных процессах тех или иных пород (известняков, серпентинитов и др.).
Зато гораздо шире в этих условиях образуется халцедон не только при процессе дегидратации гелей кремнезема, но и самостоятельным путем. Наблюдались случаи его отложения после опала в пустотах между колломорфными выделениями последнего. Наиболее широко халцедон распространен в виде кремней в известняках, а также желваков в коре выветривания, напоминающих по внешнему виду миндалины и жеоды однородного халцедона гидротермального происхождения в изверженных эффузивных породах.
При метаморфическихпроцессах кварц в значительных массах образуется при обезвоживании опалсодержащих осадочных пород с образованием так называемых яшм и слоистых роговиков (чрезвычайно тонкозернистых кварцевых и кварцево-халцедоновых пород).
Однако наибольший интерес как с минералогической, так и с практической точек зрения представляют жилы "альпийского типа", образующиеся в линзовидных трещинах, возникающих при метаморфизме и рассланцевании горных пород (см. стр. 102). В больших пустотах и трещинах ("хрустальных погребах"), лишь частично выполненных минеральным веществом, стенки бывают усеяны наросшими прекрасно образованными, нередко крупными кристаллами кварца в сопровождении хлоритов, полевого шпата, рутила, брукита и др. Эти жилы и сами кристаллы обладают многими характерными особенностями. Кристаллы горного хрусталя имеют самую различную ориентировку по отношению к стенкам пустот. Установлено, что эта ориентировка находится в зависимости от ориентировки породообразующих зерен кварца обнаженных в стенках боковой породы и явившихся затравками для крупных кристаллов, выросших в пустоте. Недеформированные кристаллы горного хрусталя обладают пьезоэлектрическими свойствами.
При процессах выветривания кварц является химически стойким минералом и потому накапливается в виде обломочных зерен в россыпях и осадочных породах (песчаниках, кварцитах).
Псевдоморфозы кварца были установлены по самым различным минералам: кальциту, бариту, гипсу, полевым шпатам, оливину и т. д., а также по животным и растительным остаткам.
Практическое значение. Применение кварца и халцедона разнообразно.
- Прозрачные красиво окрашенные разности этих минералов применяются в качестве поделочных камней для украшений.
- Бесцветные горные хрустали употребляются для изготовления оптических приборов.
- В точной механике некоторые разности этих минералов (особенно технический агат) широко используются для изготовления подпятников в механизмах, опорных призм, часовых камней и т. д.
- В радиотехнике для изготовления пьезокварцевых пластинок как стабилизаторов радиоволн, резонаторов и т. д. употребляются совершенно однородные, недвойникованные кристаллы, обладающие пьезоэлектрическими свойствами (горный хрусталь, дымчатый кварц, морион); для этих целей пригодны кристаллы размерами не менее 3,5 см между противоположными гранями призмы.
- Из плавленого кварца изготовляется химическая посуда, отличающаяся огнеупорностью и кислотоупорностью, а также кварцевые лампы, применяющиеся в медицине для лечения ультрафиолетовым светом, для которого кварц (один из немногих минералов) прозрачен.
- В стекольно-керамической промышленности для варки стекла и выделки фарфора и фаянса применяются чистые маложелезистые (до 0,002%) кварцевые пески.
- Применяется для производства карбида кремния-карборунда (SiC), обладающего высокой твердостью (выше, чем у корунда) и применяемого в качестве первоклассного абразивного материала.
- Тонкие кварцевые пески применяются в пескоструйных аппаратах для полировки поверхностей металлических и каменных изделий, а также для распиловки горных пород и для ряда других целей.
- Песчаники, состоящие из сцементированных окатанных зерен кварца, и их метаморфизованные разности-кварциты (горные породы) служат строительным материалом.
Месторождения. Из чрезвычайно многочисленных месторождений укажем лишь в качестве примеров на некоторые.
Из месторождений в СССР, представляющих большой минералогический интерес, следует отметить издавна известные Мурзинские, Липовские, Шайтанские и другие пегматитовые копи (к северо-востоку от г. Свердловска), содержащие друзы великолепных кристаллов горного хрусталя, дымчатого кварца и аметиста в ассоциации с полевыми шпатами, турмалином, лепидолитом и др. Пегматитовые жилы с морионом и аметистом распространены в хребте Адун-Чилон (Забайкалье), на Волыни (Украина) и в других местах. Месторождения кварцевых жил с горным хрусталем известны также на Алдане и Памире.
Сургучно-красные слоистые яшмы как поделочные камни распространены в Примагнитогорском районе (Урал). Широкой известностью пользуются равномерно окрашенная в зеленовато-серый цвет калганская яшма и разнообразные по рисункам яшмы Орского района (Ю. Урал).
Сколько-нибудь значительных месторождений поделочных агатов в нашем Союзе пока не известно. Месторождения так называемого технического агата встречаются в Закавказье в Ахалцихском других районах. Генетически они связаны с покровами эффузивных пород.
Из иностранных месторождений благородных разновидностей кварца следует упомянуть о месторождениях Бразилии в Минас-Жерайж и Уругвая (главным образом аметист), Мадагаскара (горный хрусталь), Швейцарских Альп и т. д. Все эти месторождения большей частью представлены пегматитовыми или кварцевыми жилами альпийского типа. Лучшие агаты известны в месторождениях Индии, Бразилии, Уругвая, Германии (Оберштейн, Рейнланд и др.).
Тридимит - SiO2. "Тридимос" по-гречески - тройной (назван вследствие часто наблюдаемых тройников). Более высокотемпературная модификация - β-тридимит гексагональной сингонии в области неустойчивых состояний легко переходит в более низкотемпературную, близкую к ней по кристаллической структуре модификацию α-тридимит ромбической сингонии. При атмосферном давлении α-тридимит с течением времени способен переходить в устойчивую форму α-кварца. Превращение β-тридимита в β-кварц, т. е. модификацию хотя и гексагональной сингонии, но весьма существенно отличающуюся по кристаллической структуре, происходит гораздо медленнее и сопровождается значительным изменением объема и удельного веса (Уд. вес β-кварца 2,51, β-тридимита-2,26).
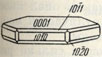
Рис. 192. Кристалл тридимита
Кристаллы α-тридимита, более устойчивого при низких температурах, наблюдаются в виде псевдогексагональных пластинок (рис. 192) или чаще тройников (рис. 193) с углом между пластинками 35°18'. Встречаются также розетковидные или черепитчатые агрегаты. Цвет α-тридимита белый, серовато-белый; иногда он бесцветный. Блеск стеклянный. Ng = 1,473, Nm = 1,470 и Np = l,469. Твердость 6-7. Спайность несовершенная. Уд. вес 2,30.
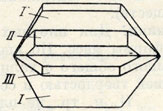
Рис. 193. Тройник тридимита
Встречается преимущественно в пустотах кислых эффузивных пород: в трахитах в Зигенгебюрге (Германия), андезитах в Сан-Кристобале (Мексика), продуктах извержений Везувия и т. д.
Кристобалит - SiO2. Название дано по местности Сан-Кристобал (Мексика). Полиморфные модификации: более высокотемпературная - β-кристобалит кубической сингонии и низкотемпературная - α-кристобалит. Этот последний относится к тетрагональной сингонии, являясь в то же время псевдокубическим.
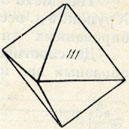
Рис. 194. Кристалл кристобалита
Кристаллы β-кристобалита обладают октаэдрическим обликом (рис. 194), реже они имеют кубическую или скелетную форму. Встречаются двойники по (111). Цвет молочно-белый. Блеск стеклянный. Nm = l,49. Твердость 7. Уд. вес 2,27.
Легко получается при образовании кварцевого стекла, а также кристаллизуется при обжиге динасовых кирпичей. Встречается в быстро остывших эффузивных породах, часто совместно с α-тридимитом: в андезитах Сан-Кристобала (Мексика), лавах Майна в Рейнланде (Германия), Иеллоустонском парке (США) - в виде шариков (сферолитов) до 1 мм в обсидиане (вулканическом стекле), а также в пустотах, иногда с наросшими пластинками тридимита на кристалликах кристобалита.
Известны и другие способы образования β-кристобалита, а именно при воздействии базальтовой магмы на кварцсодержащие осадочные породы (песчаники). Кристобалит в этих случаях образуется за счет кварца при высокой температуре. Подобные образования описаны, например, в глинистых песчаниках верхнетретичного возраста в Западной Грузии.
Опал - SiO2•аg. Типичный твердый гидрогель. Происхождение названия неизвестно. Разновидности по физическим признакам:
- благородный опал, обладающий опалесценцией;
- гидрофан - легкая разновидность, сильно пористая, мутная в сухом состоянии и прозрачная в воде;
- гиалит - сталактитовые образования или шарики сферолитового строения.
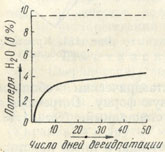
Рис. 195. Кривая обезвоживания опала над H2SО4
Химический состав очень непостоянный. Содержание воды колеблется от 1 до 5, крайне редко достигая 34%. Часть воды все опалы способны терять при высушивании в эксикаторе. Особенно быстро потеря ее происходит в первые дни (рис. 195). При нагревании одни опалы отдают главную часть воды до 100°, другие - выше этой температуры (100-250°). Причины этой различной прочности связи воды полностью не выяснены.
Морфологические особенности. Обычно наблюдается в плотных стеклоподобных массах с натечной внешней формой. Является главной составной частью некоторых организмов, слагая панцыри диатомей, спикули губок, скелеты радиолярий, отчасти некоторых фораминифер и мшанок, для которых коллоидные растворы (золи) кремнезема служат пищей. Благодаря наличию кремнезема скелеты этих организмов в большинстве случаев прекрасно сохраняются в ископаемом состоянии даже в древнейших отложениях. Гидроокислы кремнезема входят также в состав соломы злаков, твердых узловатостей в хвощах и особенно узлов бамбука и других растений, поглощающих золи кремнезема из почвы своими корнями. Золи кремнезема способны пропитывать отмершие стволы деревьев и, отлагая опал, полностью их замещать с сохранением всех деталей строения ("деревянистый опал").
Цвет. Сам по себе опал бесцветен. Благодаря различным примесям, особенно содержащим железо и другие хромофоры, он бывает окрашен в различные оттенки желтого, бурого, красного, зеленого и черного цвета. Блеск стеклянный (у пористых масс восковой или матовый). Для полупрозрачных разностей характерна опалесценция (происхождение названия этого явления связано именно с этим минералом). N=l,40-1,46.
Твердость 5-5,5 (у разностей, очень бедных водой, поднимается до 6). Хрупок. Уд. вес 1,9-2,5 (зависит от содержания воды и от количества адсорбированных тяжелых веществ).
Диагностические признаки. Для плотных опалов характерны стеклообразный вид и натечные формы масс. По внешним признакам опал имеет много общего с халцедоном. Он отличается меньшей твердостью и содержанием воды.
П. п. тр. не плавится, но часто сильно растрескивается. В закрытой трубке выделяет воду. В кислотах не разлагается. Довольно легко растворяется в КОН и HF. Обезвоженный опал растворяется в соде с шипением (вследствие выделения СO2).
Происхождение. Опал нередко отлагается из гидротермальных источников и гейзеров в вулканических областях в виде накипи (кремнистый туф, гейзерит), иногда в виде белых просвечивающих натеков с перламутровым отливом. Распространен также в пустотах и трещинах среди эффузивных горных пород, иногда в виде жеод и миндалин.
Однако в главной своей массе он образуется в экзогенных условиях при разложении силикатов в процессе выветривания самых различных по составу горных пород, но чаще ультраосновных. Кремнезем, освобождающийся при распаде кристаллических решеток силикатов, переходит первоначально в золь, при коагуляции которого выпадает в зоне элювия в виде желваков натечной формы или отлагается метасоматическим путем, часто совместно с гидроокислами железа, алюминия и других элементов, на различных коренных горных породах.
Огромные массы опала образуются осадочным путем в виде пластов в процессе коагуляции приносимых речными водами золей кремнезема в прибрежных зонах морских бассейнов. К ним принадлежат так называемые опоки, трепелы, диатомиты, кизельгур (кремневая мука) и т. д., представляющие собой рыхлые или тонкопористые, иногда более или менее крепкие породы, на поверхности часто превращенные в мелоподобные массы вследствие механического действия замерзающей воды, пропитывающей их.
Следует упомянуть, наконец, об окаменяющей роли коллоидов кремнезема при метасоматозе растительных остатков и, в частности, стволов деревьев. Каким бы путем ни образовался опал, он в конце концов постепенно переходит в халцедон или кварц.
Практическое значение. Благородные опалы употребляются как поделочные камни. Трепел применяется для полировки металлов, камней и для других целей. Кизельгур идет для изготовления фильтров, керамики, выделки легких кирпичей и для других целей.
Месторождения. Осадочные опалсодержащие породы (опоки, трепелы и диатомиты) особенно широким распространением пользуются в третичных мелководных отложениях в Ульяновской, Саратовской и других областях Европейской части СССР, а также вдоль восточного склона Уральского хребта, в Закаспии, Закавказье и в других местах. Из иностранных месторождений следует упомянуть о месторождениях Богемии, Италии, Триполи (откуда происходит название трепел) и др. Месторождения благородных опалов известны на южном склоне Карпат, близ Кошице (в пустотах изверженной породы-андезита), в Австралии - Новый Южный Уэлс и Квинсленд (в песчаниках, занимающих огромную площадь) и в других местах.
Обобщение. Таким образом, все природные модификации, за исключением опала и лешательерита (аморфного кварцевого стекла), характеризуются кристаллическими решетками, представляющими собой каркасы кремнекислородных тетраэдров, соединенных друг с другом вершинами, т. е. каждый ион кремния окружен четырьмя ионами кислорода, а каждый ион кислорода связывает два иона кремния. Отличие в структурах заключается в пространственной ориентировке этих тетраэдров. Особенности кристаллических структур обусловливают и физические свойства самих минералов (табл. 7).
| Модификация | Сингония | Уд. вес | Коэфициент преломления | ||
| Nj | Nm | Np | |||
| Стекло(кварцевое) | - | 2,204 | - | 1,460 | - |
| β-кристобалит | Кубическая | 2,21 | - | - | - |
| α-кристобалит | Тетрагональная | 2,27 | - | 1,487 | 1,48 |
| β-тридимит | Гексагональная | 2,26 | - | - | - |
| α-тридимит | Ромбическая | 2,30 | 1,473 | 1,470 | 1,469 |
| β-кварц | Гексагональная | 2,51 | - | - | - |
| α-кварц | Тригональная | 2,655 | 1,553 | 1,544 | - |
| Опал | - | 1,9-2,5 | - | 1,44 | - |
|
ПОИСК:
|
© IZNEDR.RU, 2008-2020
При использовании материалов сайта активная ссылка обязательна:
http://iznedr.ru/ 'Из недр Земли'
При использовании материалов сайта активная ссылка обязательна:
http://iznedr.ru/ 'Из недр Земли'