
Глава 13. Как определяют содержание металлов в биологических материалах
Исследование функций ионов металлов в организмах требует в первую очередь разработки точных методов качественного и количественного анализа, позволяющих обнаружить тот или иной металл и измерить его концентрацию в биологических материалах (в крови, мышечной ткани и др.). Для решения всех этих задач современная наука располагает мощным арсеналом химических и физико-химических средств исследования. За последние годы громоздкие и трудоемкие химические методы все чаще уступают место физико-химическим, основанным на явлениях поглощения, испускания, рассеяния и отражения света, избирательной адсорбции и радиоактивности. Аналитическая химия биологических материалов ныне представляет собой огромную, хорошо разработанную область науки. В рамках этой книги мы ограничимся описанием некоторых физико-химических методов, в которых важную роль играют оптические свойства исследуемых соединений.
Как правило, применению этих методов предшествуют химические процедуры, носящие подготовительный характер. Химик старается удалить из раствора все те примеси, которые мешают открытию интересующего его катиона, а когда эта работа завершена, то применяет реактив, дающий специфическое окрашивание или осадок с искомым катионом. Осадок, конечно, можно отделить, высушить и взвесить - это будет чисто химический прием. Но окрашенный раствор и даже муть в растворе с осадком можно исследовать оптическими приборами. Результат будет получен гораздо быстрее и часто с большей степенью точности.
С биологическими материалами работать трудно. Биологические объекты содержат белки, жиры, углеводы в сложных сочетаниях, и среди них в относительно малых количествах скрыты искомые ионы. Очевидно, надо избавиться от мешающих веществ. Проще всего это достигается прокаливанием органического материала, в процессе которого обугливаются белки, жиры и углеводы, а в конечном счете выгорает и уголь. Остаток можно растворить например в азотной кислоте и получить кислый раствор солей металлов (избыток кислоты легко нейтрализовать раствором аммиака). Теперь перед нами менее сложная задача - надо проанализировать неорганические вещества - соли. Качественные испытания, как правило, предшествуют количественным измерениям! Существует множество реакций, с помощью которых можно обнаружить присутствие в растворе того или иного катиона. Чаще всего пользуются реакциями образования окрашенных соединений, специфических для данного металла. Так ионы железа (III) с роданидом аммония (или калия) образуют роданид железа кроваво-красного цвета, с гексацианоферратом (II) калия-берлинскую лазурь.
Современная аналитическая химия широко использует комплексные соединения ионов металлов с различными органическими веществами. Подбирая подходящие лиганды и условия реакции, можно быстро обнаружить искомый ион даже в присутствии других ионов металлов. В таблице 7 приведены данные о характерных реакциях некоторых катионов, образующих окрашенные комплексы.
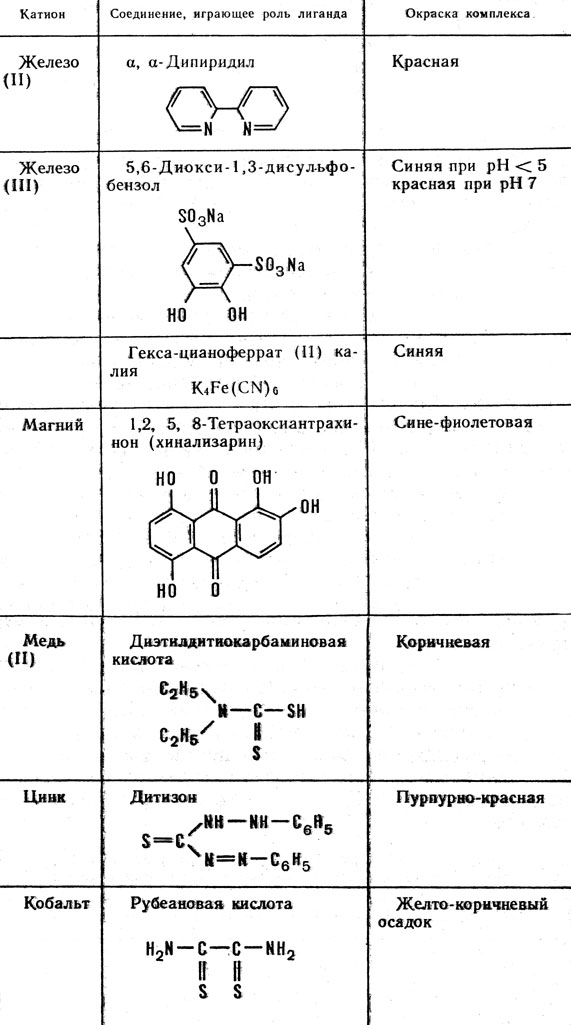
Таблица 7. Образование окрашенных комплексов, применяемых при аналитических определениях металлов
Количественные определения; следующие за качественными, часто основываются на использовании свойств указанных комплексных соединений. Дело в том" что яркая окраска комплексов, способность их интенсивно поглощать свет определенных длин волн открывает возможность измерения количества комплексного соединения фотометрическими методами.
Принцип, лежащий в основе фотометрирования, очень прост. Допустим, что ион металла переведен в комплексное соединение с какими-либо лигандами и полученное соединение ярко окрашено. Нам известно, из какого количества биологического материала получен данный объем раствора (обычно расчет ведут на 100 г материала, например на 100 г мышечной ткани), но неизвестна концентрация комплекса во всем объеме раствора.
Приготовим отдельно в чистом виде точно такой же комплекс и растворим отмеренное (известное) его количество в определенном (известном) объеме воды. Сравним окраски полученного раствора (стандарта) и исследуемого раствора. Если они одинаковы, значит и концентрации окрашенного комплекса в растворах одинаковы. А если разные, то можно приготовить такой стандартный раствор, у которого окраска будет совпадать по интенсивности с окраской исследуемого. Допустим, что исходный стандарт пришлось разбавить вдвое. Значит ли это, что исследуемый раствор имеет концентрацию вдвое меньшую, чем исходный стандарт? Да, безусловно! Но ведь можно и еще проще поступить - сравнить поглощение света в тонких слоях стандарта и данного раствора. Предположим, что стандарт поглощает больше светового излучения, чем данный раствор. Это значит, что концентрация вещества в стандарте больше. В результате тщательных исследований было доказано (закон Бугера-Ламберта-Бера), что между интенсивностью потока света Iо, падающего перпендикулярно слою раствора толщиной I, интенсивностью потока света l, прошедшего через слой раствора, и концентрацией раствора с существует математическая зависимость:
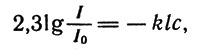
Между интенсивностью потока света Iо, падающего перпендикулярно слою раствора толщиной I, интенсивностью потока света l, прошедшего через слой раствора, и концентрацией раствора с существует математическая зависимость
где: k - коэффициент пропорциональности, характерный для данного вещества (коэффициент поглощения).
Очевидно, зная отношение I/Iо и величину k, можно вычислить и концентрацию вещества с. Длину слоя обычно берут равной единице (например 1 см). В точных приборах - спектрофотометрах - интенсивность потока света определяют по величине тока, возбуждаемого светом в фотоэлементе, поставленном за кюветой с раствором.
Целесообразно сначала измерить отношение I/Iо для ряда растворов с известным содержанием окрашенного вещества и построить график зависимости lg I/Iо от концентрации; он будет иметь вид прямой, по наклону которой к оси концентраций можно определить коэффициент поглощения. Имея такой график и зная отношение I/Iо для исследуемого раствора, легко найти и значение концентрации с.
Наша промышленность выпускает спектрофотометры с автоматической записью, в которых перо самописца вычерчивает на бумаге кривую зависимости величин логарифма отношения I/Iо от длины волны поглощаемого света. Пользуясь таким прибором, можно быстро построить калибровочный график. Для менее точных оценок применяют приборы без автоматической записи, в которых поглощение относится не к узкой области длин волн, а к широкому интервалу, выделяемому светофильтрами. Описанные устройства предназначены для исследования поглощения электромагнитных волн определенной длины, характеризующих соединения данного элемента.
Другой путь определения содержания металлов в биологических материалах заключается в изучении спектров испускания, т. е. в использовании методов спектрального анализа. Для того чтобы получить спектр испускания вещества, необходимо подвести к нему энергию - возбудить атомы. Известны различные приемы возбуждения: можно ввести вещество в вольтову дугу, в зону искрового разряда или в пламя, имеющее высокую температуру (например в ацетиленово-кислородное пламя). Полученное таким путем излучение направляют на призму спектрографа, в которой оно разлагается на узкие пучки волн различной длины; электромагнитные волны оставляют отпечаток на фотопластинке в виде ряда линий различной интенсивности. Последняя зависит от количества излучающего вещества. Сравнивая эту спектрограмму со спектрограммой, отвечающей известному количеству вещества, можно судить о концентрации изучаемого элемента в образце.
Существуют и иные методы анализа биологических материалов - все они требуют большого и кропотливого труда по подготовке образцов, но зато обеспечивают высокую точность анализов. Гораздо труднее задача - определить виды связей данного металла в биологически активных молекулах. Она отчасти также решается оптическими методами, в частности изучением инфракрасных спектров поглощения.
Исследование свойств комплексных ионов металлов ведет к раскрытию широких перспектив в биологии, практической медицине, сельском хозяйстве и позволяет разработать методы сознательного управления тонкими процессами жизнедеятельности.
Закончим на этом наш краткий обзор аналитических определений и вместе с тем закончим и книгу о металлах в организме в надежде, что читатель оценит исключительную роль металлов в поддержании жизни на Земле.
|
ПОИСК:
|
© IZNEDR.RU, 2008-2020
При использовании материалов сайта активная ссылка обязательна:
http://iznedr.ru/ 'Из недр Земли'
При использовании материалов сайта активная ссылка обязательна:
http://iznedr.ru/ 'Из недр Земли'