
Глава 8. Структурная организация мембран клетки. Окислительное фосфорилирование
Изучая некоторые этапы обмена веществ, мы рассмотрели сложные цепи реакций, в которых соблюдается вполне определенная их последовательность. Продукт одной реакции становится исходным веществом в другой; реакции включаются в строгом порядке, не обгоняя друг друга. Порядок был бы невозможен, если бы участвующие в процессе молекулы были просто смешаны в однородной среде. Действительно, микроскоп открывает перед нами необыкновенно разнообразные и тонко организованные клеточные структуры, которые играют как механическую, так и химическую роль в жизни клетки. Оболочка клетки и все детали ее внутреннего устройства образованы посредством белков и жироподобных веществ, называемых липидами. Сочетание белков и липидов приводит к возникновению макроструктур - тонких пленок, получивших название мембран.
Мембраны отделяют содержимое клетки от внешней среды и обеспечивают разницу концентраций биологически важных веществ внутри клетки и во внешней среде.
Если бы этого не было, химический состав клетки и среды стал бы одинаковым, что, конечно, нарушило бы все процессы жизнедеятельности. Мембраны способны избирательно пропускать в клетку (и в обратном направлении) определенные вещества и осуществляют таким путем контроль над количественным и качественным составом клеточного содержимого.
Химик, смешивающий в пробирке или колбе реагирующие вещества, не думает о форме сосуда, в котором идет реакция: и в колбе, и в пробирке она пройдет одинаково, сосуд не принимает участия в процессе. Клетка, с ее мембранными структурами, ведет себя иначе: в ней нет деталей, которые так или иначе не участвовали бы в реакциях; и среди них мембраны играют важнейшую роль.
По этой причине в настоящее время мембраны привлекают пристальное внимание ученых. Мембранам посвящены сотни работ, ежегодно публикуемых в печати, в нашей стране издается даже специальный журнал "Мембраны". Вопросы строения и функций этих тончайших пленок обсуждаются на конференциях и конгрессах. Можно без преувеличения сказать, что наука мембранология - это участок переднего края современной биохимии и молекулярной биологии.
Было затрачено много труда и времени на выяснение молекулярной структуры мембраны. Достигнутые результаты можно кратко суммировать так. В основном мембраны образованы молекулами липидов; на поверхности мембран находятся слабо связанные молекулы периферических белков. Другие молекулы белков (интегральные белки) погружены в липидный слой. Некоторые из них объединены в более крупные группировки - кластеры. Белковые молекулы взаимодействуют как с липидами, так и с молекулами воды внешней среды, а также в некоторых случаях и с углеводами. Для понимания причин, по которым могла возникнуть такая сложная молекулярная архитектура, надо обратить внимание на особенности строения молекул белков и липидов.
Молекулы белков, как точно установлено, состоят из остатков примерно двадцати α-аминокислот. Они имеют общую формулу NH2 - CH(R) - СООН (в нее не вписывается лишь пролин). Как видно, все аминокислоты содержат полярные группы: карбоксильные - СООН и аминогруппы - NH2, выполняющие соответственно функции кислоты или основания. Кроме того, у части аминокислот полярные группы (-СООН, -NH2, -ОН, -SH) имеются и в боковых радикалах R, тогда как у другой части R - это неполярные углеводородные цепи, прямые, разветвленные или циклические.
В процессе конденсации (см. гл. 1) образуется полипептид - длинная цепочка связанных друг с другом аминокислот:
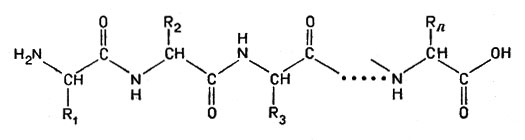
полипептид - длинная цепочка связанных друг с другом аминокислот
Именно так в клетках из различных аминокислот и получаются молекулы разнообразных белков. На боковых ответвлениях, а также на концах цепочек сохраняются кислые, основные и другие полярные группы; белки поэтому могут реагировать и с кислотами, и с основаниями.
Разнообразие белков связано с разным чередованием двадцати различных аминокислотных остатков. Поэтому число всевозможных белков необычайно велико.
Полипептидная цепочка белка, насчитывающая сотни, а иногда и тысячи звеньев, свернута в спираль, кроме того, эта спираль, в свою очередь, сложена в компактную структуру. В некоторых белках молекула содержит не одну, а две или более полипептидных цепочек, переплетенных друг с другом (например, четыре цепи гемоглобина). Отдельные части полипептидных цепей проявляют, разумеется, не одинаковые химические свойства; в частности, они по-разному относятся к молекулам воды, постоянно присутствующим в любых клетках организма. Аминогруппы -NH2 и карбоксилы -СООН, например, удерживают молекулы воды за счет образования водородной связи. Предполагается, что возникновение водородной связи облегчает отщепление ионов Н+ и ОН-:
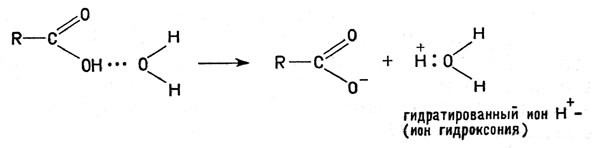
Возникновение водородной связи облегчает отщепление ионов Н+ и ОН-
Водородная связь (точки) осуществляется ионом Н+, соединенным одновременно и с атомом кислорода молекулы воды, и с атомом кислорода или азота молекулы белка. Кроме того, диполи (полярные молекулы) воды притягиваются к любому иону в растворе; поэтому те части молекул белка, которые содержат группы -ОН, -СООН, -NH2, а также -SH, вовлекаются в водную среду; их называют гидрофильными ("любящими воду").
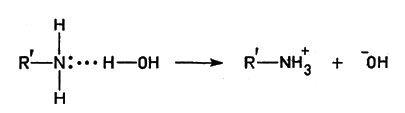
Водородная связь (точки) осуществляется ионом Н+, соединенным одновременно и с атомом кислорода молекулы воды, и с атомом кислорода или азота молекулы белка
В противоположность этому, группы углеводородного характера -(СН2)n - СН3 почти не взаимодействуют с молекулами воды (это гидрофобные группы - "боящиеся воды"). Впрочем, если несколько углеводородных цепей расположены по соседству, то они стремятся еще более приблизиться друг к другу, так как окружающие их молекулы воды, вследствие взаимного притяжения, выталкивают углеводородные цепочки из своей среды.
Эти соображения помогут нам понять, почему липиды и белки сыграли роль строительных материалов в формировании мембран. Дело в том, что липиды, при всем их разнообразии, характеризуются общими признаками. В молекулах липидов обязательно имеется длинный (чаще двойной) гидрофобный углеводородный "хвост" на другом конце его - полярная (гидрофильная) группа. На рисунке 13 изображено строение одного из липидов (фосфолипида).
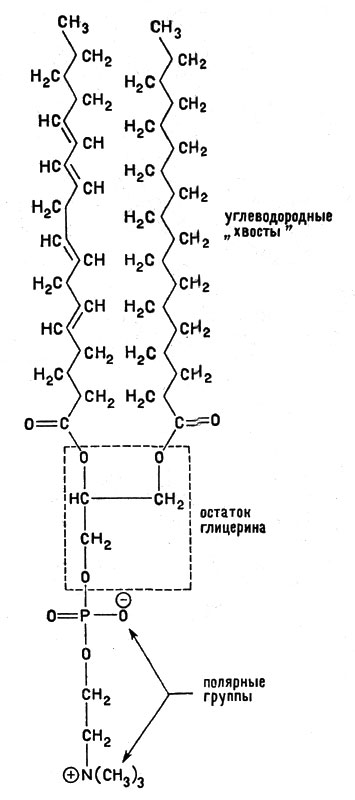
Рис. 13. Строение молекулы одного из фосфолипидов - фосфатидилхолина
Мембраны клеток построены из двух слоев липидов, обращенных друг к другу своими углеводородными частями. Гидрофильные части молекул направлены к внешней (водной) среде. Таким образом вода удерживается на обеих сторонах мембраны, а внутренние части представляют собой переплетение углеводородных хвостов липидов. В эту матрицу и погружены отдельные молекулы белков (интегральных, рис. 14). Белки, благодаря наличию у них и гидрофильных, и гидрофобных частей, могут взаимодействовать как с водной средой, так и с углеводородными цепочками липидных молекул. На поверхности мембраны гидрофильными группами удерживаются еще и периферические белки. В мембранах существуют поры, через которые могут проникать низкомолекулярные вещества. Имеются также и специальные белки-переносчики, которые переправляют через толщу мембраны строго определенные вещества, нужные клетке, и, соответственно, те, от которых она стремится избавиться.
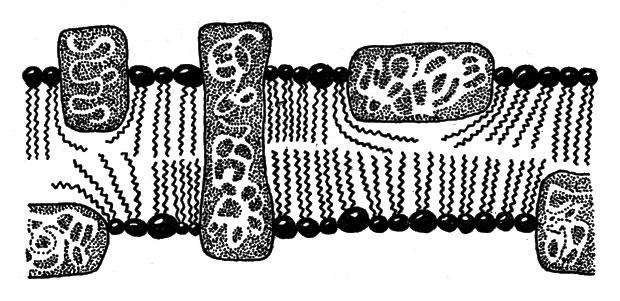
Рис. 14. Строение мембраны. В липидном слое расположены интегральные белки, снаружи слабосвязанные мембранные
Через мембраны вещество может переноситься даже и в том случае, если его концентрация растет в направлении переноса. Это кажется странным. Ведь мы хорошо знаем, что если, например, бросить сахар в воду, то сначала вокруг кусочка сахара образуется насыщенный раствор, а затем сахар распространится по всему объему воды - диффузия идет в направлении убывания концентрации. Нельзя ожидать, что раствор сахара сам собой разделится на чистую воду и чистый сахар. Вообще говоря, этого можно добиться, но обязательно затратив некоторую работу. Откуда же в клетках берется необходимая энергия, когда вещество в мембране переносится в направлении роста концентрации? Оказывается, такой активный перенос совершается за счет энергии АТФ, причем металлы выполняют в механизме переноса существенную роль.
Активный перенос - лишь один из примеров загадочного явления сопряжения процессов, сопряжения, на котором держится вся энергетика жизни. Сейчас мы и разберем данные о ходе важного сопряженного процесса - окислительного фосфорилирования, в котором реакции дыхания сопряжены с синтезом АТФ.
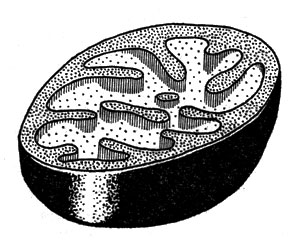
Рис. 15. Строение митохондрии (печени)
Процесс этот развертывается на мембранах митохондрий. Митохондрии - это особые органеллы клетки размером 1-2 мкм, обычно сферической или цилиндрической формы (рис. 15). Они образованы двумя мембранами: гладкой внешней и внутренней, образующей складки, или кристы, заполненные студнеобразной массой белкового характера (матриксом). На мембранах расположены различные ферменты. Особенно интересна внутренняя мембрана, на которой находятся ферменты дыхательной цепи и ферменты, обусловливающие синтез АТФ (рис. 16).
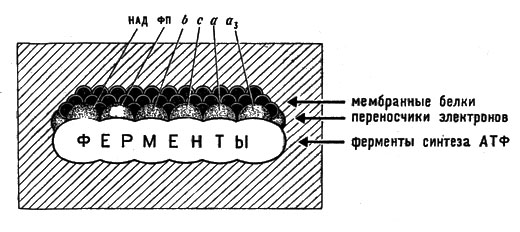
Рис. 16. Участок поверхности внутренней мембраны митохондрии. Сгруппированы все участники дыхательной цепи и синтеза АТФ
В отличие от внешней мембраны, внутренняя непроницаема для большинства низкомолекулярных веществ (для катионов натрия, анионов хлора, брома; калия, магния), а также и для НАД и НАД*Н. В матриксе находятся ферменты, обеспечивающие работу цикла Кребса (цикла трикарбоновых кислот). Кислород и вода проникают внутрь митохондрии через внешнюю мембрану путем обычной диффузии.
Предположим, что в митохондрии окисляется некоторое вещество, содержащее водород, - обозначим его АН2. В результате окисления получается вода и освобождается энергия:
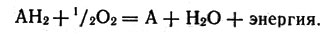
Окисление вещества, содержащее водород в митохондрии
Суть дела заключается в том, как не допустить бесполезного рассеивания этой энергии, превратить ее в энергию химических связей (аккумулировать) и до поры до времени сохранять в такой скрытой форме. Для этого служит другая реакция, а именно - образования аденозинтрифосфорной кислоты (АТФ) из аденозиндифосфорной кислоты (АДФ) и фосфата (Ф). Простейшая запись этой реакции:
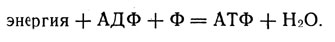
Уравнение выражает процесс аккумулирования энергии в молекулах АТФ
Это уравнение выражает процесс аккумулирования энергии в молекулах АТФ.
Весь вопрос в том, каким способом передается энергия одной реакции веществам, участвующим в другой. Предполагалось существование особых соединений - промежуточных продуктов, связывающих обе реакции. Однако обнаружить их не удалось.
В настоящее время большинство биохимиков склоняются в пользу теории П. Митчела, в которой большая роль отведена возникновению разности потенциала между внешней и внутренней сторонами мембраны митохондрий, в которых происходит образование молекул АТФ. Все события развиваются с участием мембраны, которая и является макроскопическим организатором молекулярных процессов. На рисунке 17 схематически показан этот сопряженный процесс, протекающий на поверхности и в глубине внутренней мембраны.
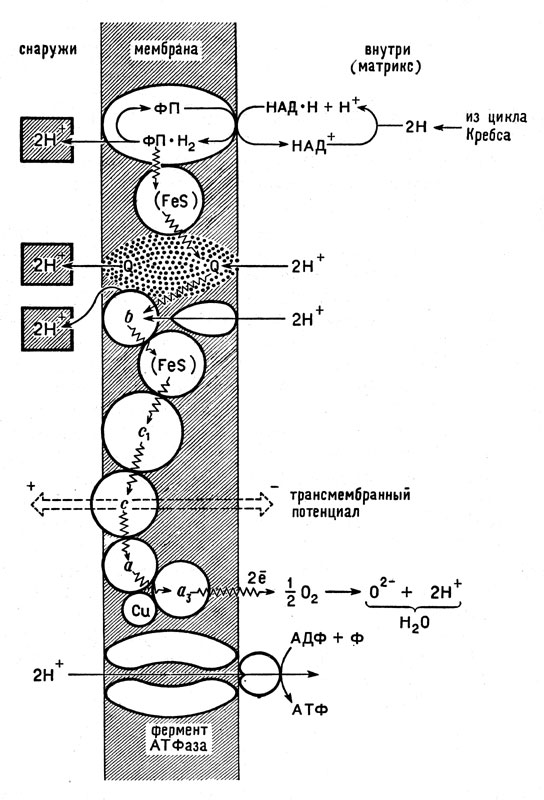
Рис. 17. Схема окислительного фосфорилирования с участием мембраны (по П. Митчелу). Волнистая линия - путь электрона; условно показано положение переносчиков электронов и фермента АТФазы
Цикл Кребса, действующий в матриксе, передает атомы водорода, отнятые у окисляемого вещества, никотин-амиддинуклеотиду (НАД), превращая его в НАД*Н + Н+. Отсюда водород переходит к флавиновым ферментам- флавопротеидам (ФП), причем восстановленная форма ФП*Н2 отдает ионы водорода Н+ другой стороне мембраны, где они могут быть частично вытеснены ионами натрия или других металлов, а электроны следуют дальше. Они попадают на железосерусодержащий (FeS) белок. Этот белок отдает два электрона двум частицам убихинона Q: присоединяя два иона водорода 2Н+ из матрикса, убихинон при этом образует соединение QH. От цитохрома b к двум частицам QH поступают еще два электрона, а из матрикса присоединяются еще два иона водорода Н+ так, что в конечном счете образуется 2QH2. Затем все четыре иона водорода уходят на другую (внешнюю) сторону мембраны, а электроны начинают движение по цепи цитохромов с1, с, а, а3, попадая в конце концов к кислороду. Заметим, что удаление водородных ионов из внутреннего пространства митохондрии ведет к понижению кислотности внутри митохондрии и повышению ее во внешней зоне.
Ионы водорода, вышедшие на внешнюю сторону мембраны, могут частично замещаться другими катионами. Все это вызывает появление разности потенциалов между двумя сторонами мембраны (трансмембранный потенциал). В нижней части рисунка 17 показано образование АТФ из АДФ и Ф.
Суммарная реакция фосфорилирования (образования АТФ), сопряженная с реакцией окисления НАД*Н, может быть записана так:
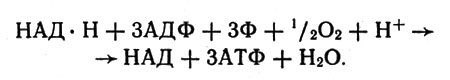
Суммарная реакция фосфорилирования (образования АТФ), сопряженная с реакцией окисления НАД*Н
Из этой схематической записи видно, что НАД*Н расстается с атомом водорода и электроном; два атома водорода и атом кислорода (точнее, 1/2 O2) образуют воду, и вместе с тем за счет энергии этого процесса из АДФ и Ф получается АТФ. Ясно, что, удаляя воду, мы сместим равновесие вправо - торону образования АТФ.
По мнению Митчела, фермент АТФ-аза, расположенный в мембране, действует так, что как только от молекул АДФ и Ф отделится молекула воды, ион Н+ втягивается через этот фермент во внутреннее пространство митохондрии (где среда слабощелочная), а ион ОН - переходит на внешнюю сторону мембраны (там среда слабокислая). На той и другой стороне перегородки происходит реакция нейтрализации.
Таким образом, разность потенциалов (разделение зарядов), наведенная в процессе дыхания в направлении, перпендикулярном мембране, является движущей силой процесса сопряженного фосфорилирования. В АТФ, в сущности, запасается энергия образования воды из водорода (отделенного от исходного пищевого вещества) и кислорода воздуха.
И во всемэтом сложном сопряженном механизме ионы металлов играют ответственную роль, обеспечивая транспорт электронов.
|
ПОИСК:
|
© IZNEDR.RU, 2008-2020
При использовании материалов сайта активная ссылка обязательна:
http://iznedr.ru/ 'Из недр Земли'
При использовании материалов сайта активная ссылка обязательна:
http://iznedr.ru/ 'Из недр Земли'