
Мир атомов
В истории науки открытие платины оставило яркий след, подорвав веру в самое святое - неподдельность золота и непогрешимость Библии, развенчав алхимию. Такими негативными результатами дело не ограничилось. Дальнейшее изучение платиновых металлов не только расширило возможности их практического применения, но и привело к нескольким поистине великим открытиям.
В 1823 году, когда свойства платины уже считали хорошо изученными, немецкий химик И. Дёберейнер продемонстрировал опыт, который выглядел как фокус и вызвал общее недоверие. Дёберейнер, выпуская из сосуда струю водорода, помещал на ее пути тонкодисперсную (губчатую) платину, и тотчас же водород загорался сам собой при комнатной температуре и даже на морозе.
Опыт повторяли многие и убедились - подвоха нет. Сколько бы раз ни воспламеняли струю, сколько бы времени ни горел водород, платина у контакта с ним остается неизменной, сохраняя свой вес, вид, свойства. Следовательно, она не участвует в реакции, так почему же тогда, соприкасаясь с ней, загорается водород? Почему нагревается платина?
Объяснить это не смог тогда никто, за исключением, как иронически отметил автор открытия, сторонников старой версии о том, что платина - творение бесовское. Не пытаясь их опровергнуть, Дёберейнер сосредоточил усилия на практическом использовании замечательного свойства, создав водородное (или дёберейнерово) огниво - свинцовый сосуд, в котором серная кислота, реагируя с цинком, образует водород. Его струя, при выходе из крана, соприкоснувшись с платиновой пластинкой, загоралась. Горение прекращали, закрыв кран. При этом давление газа в сосуде возрастало, оттесняя кислоту от цинка, и образование водорода прекращалось, пока кран вновь не будет открыт.
Такой быстрый и безопасный способ получения огня до изобретения спичек пользовался широким распространением. Огниво сумели "миниатюризировать" почти до размера современной зажигалки.
Новое свойство платины привлекло общее внимание, и тут выяснилось, что первым, правда в менее эффектной форме, его подметил X. Дэви, обнаруживший в 1818 году, что в присутствии платины кислород самопроизвольно превращает винный спирт в уксусную кислоту.
Вскоре Дёберейнер продемонстрировал еще один эффектный опыт: он взрывал гремучий газ, приближая к нему платину, как волшебную палочку.
В те же годы другие исследователи установили, что способность возбуждать химические реакции, замедлять их или ускорять не является уникальной особенностью платины, а присуща и некоторым другим элементам и соединениям.
Берцелиус в 1835 году предложил вещества, обладающие таким свойством, называть катализаторами (от древнегреческого: разлагать, возбуждать).
Вслед за огнивом были изобретены каталитические грелки. Они применяются и поныне: горючее из резервуара по фитилю подводят к платиновому катализатору. Под его влиянием, взаимодействуя с кислородом воздуха, горючее окисляется и порождает тепло без образования пламени, при безопасной для воспламенения температуре.
В конце прошлого века был придуман контактный способ получения серной кислоты путем окисления сернистого газа на платине. Для экономного ее расходования применили "пушонку" - тончайшие волокна асбеста, покрытые платиновой чернью.
С той поры катализаторы, платиновые и другие, применяются все шире (об этом будет еще речь) и во многом обусловили прогресс химической технологии, хотя причины их "магического" действия прояснялись очень медленно, вместе с ростом знаний о строении вещества. Основа этих знаний - периодическая система элементов Д. И. Менделеева. Сущность ее общеизвестна и не требует пояснений. Здесь надо лишь отметить особую роль платиновых металлов в ее рождении. Химия тогда представляла" по существу, лишь набор разрозненных сведений об элементах и их соединениях. Попытки систематизации базировались в основном на внешних признаках и успеха не приносили.
Открытие Волластоном и Теннантом четырех элементов, спутников платины, вызвало предположения о том, что соседство их не случайно, а обусловлено химической общностью, но доказать родство могли только очень глубокие и трудные сопоставительные исследования. Выполнить их смог только К. К. Клаус. Открытый им рутений внес как бы симметрию в строение семейства, заполнил недостающее звено. Накопленные за 20 лет упорного труда данные позволили Клаусу обосновать, что все эти металлы по своим химическим свойствам "являются членами нераздельной хорошо образованной группы".
Результаты исследований Клауса привлекли особое внимание Д. И. Менделеева. В 1869 году он опубликовал книгу "Основы химии", которая навсегда стала подлинной основой не только химии, но и всех наук, изучающих строение вещества. В ней Менделеев особо отметил, что в открытии периодической системы путеводной нитью послужило "замечательное сходство между рядами Pd-Rh-Ru и Pt-Ir-Os ... установленное казанским профессором Клаусом".
Следует напомнить и о том, что платиновые металлы, послужив "путеводной нитью", вскоре обратились в "твердый орешек", когда пришлось Менделееву решать, где же их место в периодах и группах системы.
Данные о свойствах платиновых металлов приведены в таблице 1.
Таблица 1. Основные свойства платиновых металлов
| Свойства | "Тяжелые" | "Сверхтяжелые" | ||||
| Рутений | Родий | Палладий | Осмий | Иридий | Платина | |
| Атомный номер | 44 | 45 | 46 | 76 | 77 | 78 |
| Атомный радиус в ангстремах (10-8 см) | 1,31 | 1,34 | 1,37 | 1,32 | 1,35 | 1,38 |
| Атомная масса | 101,1 | 102,91 | 106,4 | 190,2 | 192,2 | 195,09 |
| Валентность | 0, +1, +2, +3, +4, +5, +6, +7, +8 | +1, +2, +3 | +2, +3, +4 | +2, +3, +4, +6, +8 | +1, +2, +3, +4, +6 | +2, +3, +4 |
| Плотность при 200 С (г/см3) | 12,30 | 12,42 | 11,90 | 22,7 | 22,65 | 21,45 |
| Температура плавления (0С) | 2400 | 1960 | 1555 | 2700 | 2443 | 1769 |
| Температура кипения (0С) | 4200 | 3900 | 3170 | 5300 | 4560 | 4400 |
| Твердость по Моосу | 6,5 | 6 | 4,2-5 | 7 | 6,5 | 4,1 |
| Твердость по Бринеллю (кгс/мм2) | 193,6 | 55 | 31,7 | - | 163 | 30,5 |
| Кристаллическая структура | гексагональная | кубическая | кубическая | гексагональная | кубическая | кубическая |
Бросается в глаза наиболее четкое различие: членов семейства можно, почти по Чехову, подразделить на "тонких" и "толстых" или на "тяжелых" и "сверхтяжелых" (по принятой в науке классификации).
При создании периодической системы Д. И. Менделеев построил все элементы в шеренгу по атомному весу, или, применяя современную терминологию, по их атомным номерам. Семейство платиноидов оказалось в этом строю разорванным на две триады: рутений (№ 44), родий (№ 45), палладий (№ 46) и осмий (№ 76), иридий (№ 77), платина (№ 78). Разделяют их тридцать иных элементов, и, следовательно, место этим триадам в разных периодах системы.
Обнаружилась неоднородность семейства и по другому важному признаку - валентности. Она определяет поведение веществ в химических реакциях, и Менделеев по этому критерию выделил в системе группы, объединив в каждой из них элементы с одинаковой максимальной валентностью, равной номеру группы.
Данные о валентности показывают, что и по этому признаку семейство должно быть расчленено, но уже не на триады, а, так сказать, поперек, с отделением восьмивалентных рутения и осмия, а также шестивалентного иридия от остальных.
Так существует ли вообще семейство?
Веским аргументом в его защиту явилось то, что триады при всей их разобщенности во многом сходны, и у каждого "легкого" элемента есть очень на него похожий тяжелый "брат", занимающий в строю аналогичное место. Поэтому триады могут быть объединены и разделены по вертикали на три диады. Так, "левофланговый" первой триады рутений по многим признакам сходен с "левофланговым" второй триады осмием, оба они отличаются от остальных своей структурой, самой высокой температурой плавления, наибольшей твердостью и хрупкостью, устойчивостью к кислотам и легче всех других соединимы с кислородом. Такую же близость обнаруживают и следующие пары: родий с иридием, палладий с платиной. Отчетливо и то, что свойства элементов в обеих триадах изменяются закономерно - от диады к диаде возрастает химическая стойкость, снижаются температуры плавления и твердость.
Все это, как и многочисленные примеры сходного поведения платиноидов при различных химических реакциях, подтверждало, что они не случайные соседи в природе, а подлинные "родственники", и это в периодической системе должно быть отображено. При ее построении выявилось, что каждая триада имеет на своем правом фланге "законных" соседей: палладий (№ 46) граничит с серебром (№ 47) и платина (№ 78) с золотом (№ 79), а на противоположном фланге соседей не оказалось, там рядом с рутением (№ 44) и осмием (№ 76) пустовали "квартиры", предназначенные для элементов № 43 и № 75.
Какими они окажутся? Может быть, где-то затаилось еще два платиноида и их семейство включает не шесть, а восемь членов и состоит не из двух триад, а из двух тетрад?
Возможно и другое. Судя по положению в периодической системе, могут быть в родстве с марганцем и молибденом эти неизвестные элементы. Менделеев условно назвал их экамарганцем и двимарганцем (на санскритском языке "эка" - один, "дви" - два), показав таким образом, какое предположение он считает более вероятным.
После долгих раздумий, отвергнув много вариантов, Менделеев признал, что черты сходства между платиновыми металлами являются определяющими, а различия еще ждут своего объяснения.
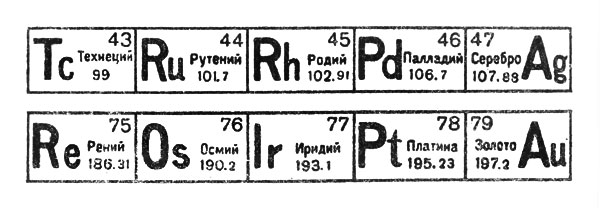
Семейство платины и его соседи
Менделеев решил отнести все платиноиды, вне зависимости от установленной максимальной валентности, к VIII группе и разделить их в отличие от остальных на три подгруппы. Так он отразил особенность "триадного" строения семейства, а симметричным расположением триад в 5 и 6 периодах показал их взаимосвязь.
Все это вызвало споры. Многие исследователи считали, что Менделеев поспешил, согласившись с Клаусом. Предполагая, что Озанн был на верном пути, они продолжали поиск новых элементов в платиновой руде, и это не раз порождало сенсации. В 1877 году был обнаружен "дэвий", а два года спустя "уралий", затем "люций" и "ниппоний". В 1903 году родился "америлий", а в 1911 - "канадий". Ни одно открытие не подтвердилось, за новый элемент принимали различные соединения иридия и родия (что иллюстрирует, как трудно их изучение).
Лишь в 1925 году, направив поиск по иному пути, Вальтер Ноддак и Ида Такке (впоследствии Ноддак) после трех лет упорного труда выявили сначала в молибденовой, а затем и в марганцевой руде ничтожное содержание элемента № 75 - рения. А № 43 оставался загадкой до 1937 года, когда итальянский физик Эмилио Сегре доказал его существование и назвал технецием (искусственным, по-гречески), что вполне отвечало сути: элемент был получен при бомбардировке молибдена ядрами тяжелого водорода - дейтерия в циклотроне.
Рений и технеций по ряду признаков оказались близкими к молибдену и марганцу, и это завершило спор о численности платинового семейства. Другой спор - о его месте в периодической системе - продолжается, и попытки модернизировать таблицу Менделеева делались неоднократно. Получил распространение, например, ее вариант, где в VIII группе оставлены только рутений и осмий, а остальные платиновые металлы вместе с кобальтом и никелем помещены по соседству, но за пределами таблицы (что ничего не меняет по сути).
Причины различной валентности, как и многие иные особенности элементов, Д. И. Менделеев при уровне знаний его времени установить не мог и ограничился такими словами: "Легко предположить, но ныне пока еще нет возможности доказать, что атомы простых тел суть сложные вещества, образованные сложением некоторых еще меньших частей..."
Все это уже доказано, и накопленные знания позволяют объяснить многое.
Современные представления об атомном строении платиновых металлов отображены в таблице 2. Она требует некоторых пояснений.
Таблица 2. Атомное строение платиновых металлов
| Элементы | Ядро | Электронные оболочки | |||||||||||||||
| Протоны | Нейтроны | K | L | M | N | O | P | ||||||||||
| 1s | 2s | 2p | 3s | 3p | 3d | 4s | 4p | 4d | 4f | 5s | 5p | 5d | 5f | 6s | |||
| Ru | 44 | 50-63 | 2 | 2 | 6 | 2 | 6 | 10 | 2 | 6 | 7 | - | 1 | * | * | * | * |
| Rh | 45 | 52-65 | 2 | 2 | 6 | 2 | 6 | 10 | 2 | 6 | 8 | - | 1 | * | * | * | * |
| Pd | 46 | 52-67 | 2 | 2 | 6 | 2 | 6 | 10 | 2 | 6 | 10 | - | - | * | * | * | * |
| Os | 76 | 106-116 | 2 | 2 | 6 | 2 | 6 | 10 | 2 | 6 | 10 | 14 | 2 | 6 | 6 | - | 2 |
| Ir | 77 | 114-116 | 2 | 2 | 6 | 2 | 6 | 10 | 2 | 6 | 10 | 14 | 2 | 6 | 7 | - | 2 |
| Pt | 78 | 110-122 | 2 | 2 | 6 | 2 | 6 | 10 | 2 | 6 | 10 | 14 | 2 | 6 | 8 | - | 2 |
"Лицо" элемента и его место в периодической системе определяет заряд ядра - число протонов, которое присуще только ему и неизменно, пока живет атом. Количество нейтронов в ядре фиксировано не так строго, оно может быть в пределах, указанных в таблице. Это обусловливает существование изотопов, атомов-"близнецов", одинаковых по химическим свойствам, но разных по атомной массе и продолжительности жизни.
Все природные изотопы платиновых металлов стабильны, являются долгожителями и мирно сосуществуют. Однако теперь к ним добавились "рукотворные" (радиогенные) изотопы, которые живут мало, но представляют для человечества большую опасность (о них тоже будет еще разговор).
Изучение строения атомов выявило причину уникальной тяжести платины, иридия, осмия и резкого их отличия по этому признаку от остальных "родственников".
"Электронное облако", окружающее ядро, почти невесомо, и масса атома определяется суммой протонов и нейтронов. Она у металлов триады платины почти вдвое больше, чем у их аналогов триады палладия. А объем атомов у всех платиноидов почти одинаков и по сравнению со многими другими металлами очень мал. Плотность вещества определяет соотношение массы атома и его объема. Масса наиболее распространенного изотопа платины - 195, а золота - 197, но платина тяжелее потому, что ее масса "втиснута" в меньший атомный объем (он равен 9,1 см2/г-атом, а у золота - 10,2). У осмия и иридия соотношение между массой и объемом атома еще лучше - соответственно 190:8,5 и 192:8,6, и они чемпионы. Наиболее насыщено протонами и нейтронами ядро урана - 238, но "квартира" велика - 12,6 см2/г-атом, и поэтому элемент с самым тяжелым в природе ядром соревнование проигрывает, его плотность "всего лишь" 19,0 г/см3.
Устойчивость любого атома обусловливается равенством между числом положительно заряженных протонов ядра и окружающих его электронов, несущих отрицательный заряд. Строение "электронного облака" неравномерно, орбиты движения ориентированы в пространстве и группируются в оболочки, каждая из которых предельно может вмещать 2n2 электронов, где n - номер оболочки, считая от ядра. (Первая оболочка вмещает 2, вторая 8, следующие 18, 32, 50 и т. д. электронов. В таблице 2 показано их распределение на различных энергетических уровнях каждой оболочки.)
Как известно, металлы отличаются от неметаллов малым числом электронов на внешней оболочке, что обусловливает их легкий отрыв и превращение "нейтральных" атомов в положительно заряженные ионы. Интенсивность таких процессов во многом определяется строением "предвнешних" оболочек. По этому признаку выделяют "непереходные" элементы - у них на всех внутренних оболочках полный комплект электронов, они как бы "связаны" и неспособны помогать своим коллегам, "сражающимся" на передовой.
Такие элементы не стойки и легко утрачивают самостоятельность. В отличие от них у элементов, называемых переходными, не все внутренние уровни заполнены электронами, и они способны перемещаться, становиться валентными. При этом из глубин атома как бы происходит приток свежей "силы". Установлено, что среди переходных элементов лучшими технологическими свойствами обладают те, у которых не полностью заполнен уровень d (вольфрам, молибден, рений и др.). К таким d-элементам принадлежат и все платиновые металлы (с оговоркой, что палладий имеет такое строение только в ионизированном состоянии). Важное отличие платиноидов, а также золота и серебра от других d-элементов заключается в том, что у них при малом заполнении уровня d совсем не заполнен "предвнешний" уровень f. Такое сочетание обусловливает особо широкий диапазон перемещения электронов и большую энергию связей. Это отличает благородные металлы от всех иных.
Строение атомов объясняет загадочную особенность рутения, выявленную еще Клаусом. Оказалось, что по разнообразию валентности рутений - чемпион. Известны соединения, в которых она равна нулю - Ru(CO)n, единице - Ru(CO)nBr, двум, трем, четырем - RuO2 (это наиболее распространенный вид соединений), а также пяти... и т. д. до восьми - RuO4. Но и этими - девятью! - валентностями его способность, как оказалось, не ограничена. Клаусом были получены соединения, строение которых не удавалось объяснить обычными представлениями о валентности.
В конце прошлого века швейцарский химик А. Вернер, развив представления Клауса, создал основы теории комплексных соединений, в которых центральное место занимает атом металла - рутения, платины и других "склонных к комплексообразованию", способных крепко удерживать не только отдельные атомы, но и лиганды - различные их соединения (радикалы, молекулы неорганические и органические). Строение таких комплексов определяется координационным числом, отражающим, какое количество лиганд центральный атом может удержать.
Представления Вернера получили обоснование и блестящее развитие в трудах Льва Александровича Чугаева. Он создал много комплексных соединений платины, палладия, никеля и установил, что все они по своей структуре аналогичны органическим соединениям. Стереохимическими построениями он выявил закономерность расположения лиганд в пространстве и обосновал "правило циклов", позволяющее целенаправленно создавать наиболее устойчивые комплексы.
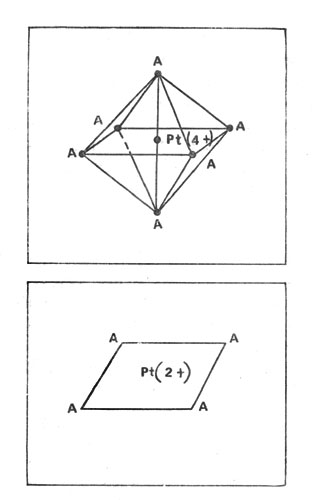
Схема строения платиновых комплексов (буквой А обозначены лиганды)
В дальнейшем развитии химии комплексных соединений очень велика роль академика Ильи Ильича Черняева и многих других советских исследователей (Ю. Н. Голованова, А. А. Гринберга, О. Е. Звягинцева, Б. Г. Карпова, В. В. Либединского, Н. К. Пшеницына, Н. М. Синицына, С. М. Старостина, П. И. Рожкова, Э. X. Фрицмана ...). Они не только усовершенствовали методы получения платиновых металлов, но и создали сотни их соединений, не существующих в природе, расширив тем самым возможности химии и техники. Глубоко разработана ими теория комплексных соединений. Установлено, что платиновые металлы - лучшие комплексообразователи, вступающие в сложные связи - ковалентные, дативные, в которых участвуют не одна, а несколько пар электронов. Причина этого - незастроенность уровня d, она особо резко выражена у рутения, что и определяет его "чемпионство" (уже получены нитрозосоединения рутения с восемнадцатиэлектронной конфигурацией молекул, обладающие уникальной термической и химической стойкостью). Имеют важное применение и комплексные соединения родия, но на первом месте и по количеству (их сотни), и по практическому значению комплексы, основу которых составляет платина.
Значение комплексных соединений в науке и технике так велико, что к числу важнейших "заслуг" платиноидов надо в один ряд с открытием периодического закона и явлений катализа поставить и координационную химию.
С помощью рентгеновских, электронных и других способов проникновения вглубь вещества установлено, что многие свойства обусловлены не особенностями отдельных атомов, а строением их совокупности - кристаллов. Они возникают под воздействием сил связи между атомами и характерны расположением их в определенном порядке, который неодинаков по разным направлениям. Чем интенсивнее эти силы, тем плотнее соприкасаются атомы. Самая плотная их упаковка достигается при кубической гранецентрированной структуре, где каждый атом окружен 12 ближайшими соседями - восемь атомов расположены в вершинах куба и еще шесть по одному в центре каждой его грани. Такое строение имеют платина, иридий, палладий, родий, а также золото, серебро, свинец и некоторые другие металлы. Рутений и осмий обладают менее совершенной гексагональной структурой, что и обусловливает меньшее их по сравнению с другими членами семьи "благородство".
Атомы металлов, если их сравнивать с атомами других элементов, обладают наибольшей силой связи. Вследствие этого они сближены так, что их внешние оболочки перекрывают друг друга. Это облегчает отрыв валентных электронов и превращение в узлах кристаллической решетки нейтральных атомов в положительно заряженные ионы. Оторвавшиеся электроны мчатся с непостижимой скоростью (20000 км/сек), бомбят ионы, превращая их на миг в атомы и снова ускользая. Непрерывный обмен "коллективизированными" электронами обусловливает пластичность металлов. При относительном перемещении ионов связь их с такими электронами не ослабевает, и поэтому изменение формы тела происходит без разрушения. Платина в этом отношении - чемпион, предел, до которого может быть растянута ее нить, еще не установлен.
Высокая электропроводность металлов также обусловлена "коллективизированными" электронами. В "нейтральном" металле они перемещаются по всем направлениям равномерно, но при подключении к источнику электроэнергии их движение становится направленным к положительному полюсу и скорость возрастает. По сравнению с веществами, не имеющими свободных электронов, проводимость металлов больше в 1025 раз. Наилучшей проводимостью обладают серебро, медь, золото. Платиноиды им уступают, но у них самое низкое значение величины удельного электросопротивления.
Способность металлов проводить теплоту при нагревании пропорциональна их электропроводности, потому что тепло тоже в основном передается электронной средой. У неметаллов, в которых тепло распространяется лишь колебанием ионов и атомов кристаллической решетки, теплопроводность в тысячу раз ниже. При нагреве возрастают колебательные движения ионов и соответственно затрудняется движение "коллективизированных" электронов. Это приводит к росту электрического сопротивления (у платиноидов оно возрастает в 3-5 раз при температурах, превышающих 1200° С). С повышением температуры теплопроводность снижается у всех платиновых металлов, за исключением самой платины (объяснение этому еще не найдено).
Энергией межатомных связей определяется тугоплавкость металлов - качество, необычайно важное для современной техники, работающей в условиях высоких температур: головные части ракет, пробивающие плотные слои атмосферы, сопла ракетных двигателей и газовых турбин и т. д. Чем выше температура, тем сильнее раскачивается кристаллическая решетка, и металлы, имеющие, например, гексагональное строение, расширяясь резко неодинаково по различным направлениям, быстро разрушаются. Среди металлов наиболее устойчивой, кубической структуры самые выносливые те, у кого энергично работают электроны с уровня d. Чемпион по тугоплавкости - вольфрам (3380° С), но он не жаростоек. Уже при 700° С вольфрам начинает "потеть", покрывающая изделия прочная пленка его окисла улетучивается.
Поэтому он чемпион лишь в условиях вакуума или в атмосфере инертных газов, а во всех более трудных условиях незаменимы платиноиды.
Долгое время металлы удавалось сопоставить только по их физическим свойствам (плотность, твердость, магнитность и т. д.). Этого недостаточно, чтобы предвидеть их поведение при различных химических процессах. Разработать объективный критерий для сопоставления "силы" металлов, их активности, удалось харьковскому профессору Н. И. Бекетову. В 1865 году он опубликовал "Исследования над явлением вытеснения одних элементов другими", в которых приведены результаты воздействия водорода на соли различных металлов, что позволило построить "вытеснительный ряд" по скорости и направленности процесса (теперь его называют "электрохимическим рядом напряжений", последовательность в котором определяется величиной энергии, необходимой, чтобы оторвать от атома один электрон). По трудности этого отрыва платина вместе с золотом стоят на самой высокой ступени. Бекетов присудил платине "пальму первенства" как сочетающей в себе химическую стойкость золота, тепло- и электропроводность серебра и превосходящей их по механической прочности и жаростойкости.
Познание строения вещества несколько прояснило причины "магического" воздействия катализаторов. Установлено, что для них типична разнообразная конфигурация кристаллов, ступенчатость их строения, расположение атомов не только на плоских гранях, но и на ребрах, где они окружены меньшим числом соседей и способны взаимодействовать особенно энергично. Как показали специальные исследования, у платины, например, активность атомов, расположенных на ребрах, в 60 раз выше, чем у тех, что находятся на гранях.
Благодаря высокой энергии поверхностных электронов, катализаторы при соприкосновении с другими веществами вступают в мгновенные взаимодействия, разрывают их молекулы и тут же восстанавливают свои состав (такие взаимодействия называют промежуточными).
Каталитические свойства наиболее ярко проявлены у d-элементов; среди них платина резко выделяется широтой энергетического спектра атомов и разнообразием их позиций, что и определяет ее замечательную активность при самых разнообразных процессах.
У многих других катализаторов, в том числе и у платиноидов, эти качества проявлены более узко, что и обусловливает избирательность их каталитического воздействия.
Далеко еще не все особенности платиноидов получили свое объяснение, в их числе феноменальная способность рутения и палладия сорбировать водород (до 1500 кубических сантиметров его в одном кубическом сантиметре), но в целом успехи в познании платиновых металлов очень велики и значительно расширили возможности рационального их использования.
|
ПОИСК:
|
© IZNEDR.RU, 2008-2020
При использовании материалов сайта активная ссылка обязательна:
http://iznedr.ru/ 'Из недр Земли'
При использовании материалов сайта активная ссылка обязательна:
http://iznedr.ru/ 'Из недр Земли'