
Углерод многоликий
Углерод многоликий
Алмаз известен людям с незапамятных времен. Старинные легенды позволяют предполагать, что первые находки алмазов в Индии относятся к третьему тысячелетию до нашей эры. Не менее чем за пять веков до начала современного летосчисления с алмазом познакомились древние греки, поскольку к этому времени относится греческая бронзовая статуэтка, глазами которой служат два неотшлифованных алмаза. Высказываются предположения, что в Грецию алмазы были завезены из Индии. В Европу заметное количество индийских алмазов начало поступать только в XIII в. Долгое время исключительно высокая твердость камня являлась непреодолимым препятствием для европейских ювелиров, и все попытки обработать этот минерал терпели неудачу. Лишь в середине XV в. голландцу Ван-Беркену удалось огранить алмазы, шлифуя их друг о друга. Долго оставался неизвестным и химический состав таинственного камня, не поддававшегося воздействию самых сильных кислот и щелочей. Некоторые ученые даже думали, что алмаз состоит из особого химического элемента - алмазной земли. В середине XVII в. во Флоренции ставились опыты по нагреванию в закрытых сосудах алмазов и рубинов. При этом было установлено, что рубины не претерпевали никаких изменений, а от алмазов не оставалось "ни малейшего следа". Это казалось совершенно необъяснимым, и лишь много позднее выяснилось, что кристаллы алмаза, нагреваемые в окружении кислорода, попросту сгорают.
Показательное сжигание алмаза в конце XVIII в. было проведено в Петербургском горном училище (ныне Ленинградский горный институт). Этот опыт, по-видимому, имел целью доказать невозможность искусственного получения крупных алмазов путем сплавления мелких кристаллов. К этому же времени относятся многочисленные опыты по сжиганию алмазов, проводившиеся в различных странах Западной Европы.
Большое внимание этим опытам уделял и знаменитый французский химик А. Лавуазье, поскольку "бесследное" исчезновение алмаза при нагревании противоречило закону сохранения материи. Он смог определенно сказать лишь то, что алмаз принадлежит к классу горючих тел и что продуктом сгорания его является газообразное вещество. Отметив возможное родство алмаза с углеродом, ученый все же не решился отождествить сверкающий камень с углем и не сделал окончательного вывода о составе алмаза. Он писал, что, может быть, никогда нельзя будет определить состав этого минерала.
Однако уже на рубеже XVIII и XIX вв. химическая природа алмаза была точно установлена. Английский химик П. Теннан в 1797 г. сжег алмаз в плотно закрытом золотом сосуде, заполненном кислородом, и установил, что образовавшийся при этом газ является двуокисью углерода. Поскольку первоначально в сосуде кроме алмаза и кислорода ничего не было, то, следовательно, алмаз в химическом отношении является чистым углеродом. Чтобы окончательно убедиться в правильности сделанного вывода, П. Теннан определил количество углерода в заполняющем сосуд углекислом газе. Оказалось, что оно в точности соответствует массе сгоревшего алмаза.
Таким образом, алмаз состоит из одного химического элемента - углерода. Аналогичный химический состав (не считая случайных и механических примесей) имеют графит, древесный и каменный уголь, сажа, т. е. весьма распространенные и далеко не самые привлекательные по внешнему виду вещества. А если это так, то в чем же причина совершенно различного облика столь разных физических и химических свойств этих веществ?
Исключительную по своей прозорливости мысль высказал М. В. Ломоносов: причиной необычайной твердости алмаза является "сложение его из частиц, тесно соединенных". Предвидение гениального ученого подтвердилось почти через два столетия, в начале XX в., когда с помощью рентгеновских лучей удалось расшифровать атомную структуру алмаза и графита. Были установлены существенные различия в пространственном расположении слагающих эти вещества элементарных частиц - атомов.
В алмазе атомы углерода размещаются очень плотно, причем каждый из них прочно связан с четырьмя окружающими его атомами (рис. 13).
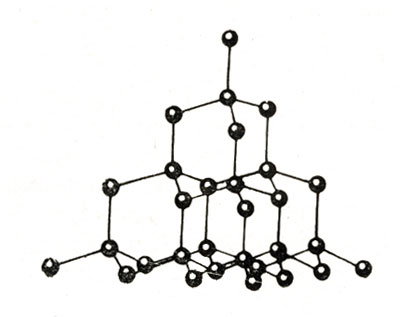
Рис. 13. Атомная структура алмаза
Совершенно иной вид имеет кристаллическая решетка графита. Структура ее образована параллельными слоями сеток, состоящих из шестиугольников с атомами углерода в вершинах. Слои отстоят на 3,39 Å (Å - сокращенное обозначение единицы длины, равной 10-8 см, которая называется "ангстрем") один от другого и последовательно сдвинуты, так что в проекции совмещается только половина атомов углерода, а остальная часть их проецируется в центре ячеек сетки нижних и верхних слоев (рис. 14). Связь между слоями атомов в графите осуществляется посредством легкоподвижных электронов. Такая связь придает веществу металлические свойства: непрозрачность, блеск, высокую электропроводность. Атомы в каждом отдельно взятом слое связаны достаточно прочно, а связь между слоями слабая. Этим обусловливается весьма высокая способность расщепляться на тонкие пластинки и чрезвычайно малая твердость графита по направлению, параллельному слоистости кристаллической решетки минерала.
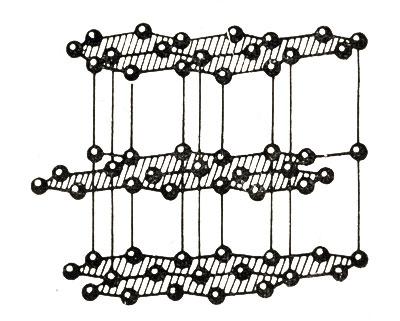
Рис. 14. Атомная структура графита
Образование одинаковых по химическому составу веществ, различающихся кристаллической структурой решетки, называется полиморфизмом, а сами такие вещества называются полиморфными модификациями. Следовательно, алмаз и графит являются полиморфными модификациями углерода.
Рассмотрим важнейшие свойства алмаза и проследим их связь с внутренним строением минерала.
Хотя алмаз в чистом виде состоит только из атомов углерода, реальные природные кристаллы этого минерала постоянно содержат примеси других веществ. Минимальные количества примесей характерны для бесцветных и слабоокрашенных прозрачных алмазов. При сжигании таких камней количество золы не превышает 0,02-0,05% от их массы. В замутненных и особенно в непрозрачных разновидностях алмаза содержание золы достигает нескольких процентов.
Спектральным анализом в составе золы установлены кремний, магний, кальций, алюминий, железо, титан и некоторые другие химические элементы.
Наряду с мельчайшими включениями в алмазах нередко присутствуют и сравнительно крупные посторонние частицы: чаще всего графит, несколько реже минералы, являющиеся по химическому составу силикатами (оливин, пироксены), алюмосиликатами (гранаты) и сложными окислами (хромшпинелиды). В крупных кристаллах алмаза довольно обычны также включения его мелких кристалликов.
Плотность алмаза около 3,52. Эта величина типична для чистых хорошо образованных кристаллов. У мелкозернистых агрегатов, часто содержащих включения графита и обладающих не вполне массивным сложением, плотность существенно ниже и у отдельных разновидностей карбонадо опускается до 3,0. Для сравнения укажем, что плотность графита не превышает 2,23. Таким образом, "рыхлость" атомной структуры графита привела к более чем полуторакратному снижению плотности.
Цвет и особенности светопреломления алмаза рассмотрены в предыдущей главе, а здесь мы остановимся еще на одном весьма интересном и важном его свойстве, которое также тесно связано с внутренним строением. Речь пойдет о люминесценции. Люминесценцией называется способность некоторых природных и синтетических веществ светиться под действием рентгеновских, ультрафиолетовых и катодных лучей, что принято обозначать специальными терминами: рентгенолюминесценция, фотолюминесценция, катодолюминесценция.
Большинство алмазов обладает всеми тремя видами люминесценции. Некоторые кристаллы при этом светятся голубым, другие зеленым, желтым или розовым светом. Темноокрашенные (бурые, черные и т. п.) и ожелезненные кристаллы, а также некоторые прозрачные их разновидности не люминесцируют.
Наиболее изучены рентгено- и фотолюминесценция алмаза, которые используются при проведении геологопоисковых работ, о чем подробнее рассказывается в заключительных главах. Некоторые исследователи связывают люминесценцию с присутствием посторонних примесей, другие указывают на причинную связь этого явления со специфическими особенностями кристаллической решетки минерала.
Чистые кристаллы прозрачны не только для световых, но и для рентгеновских лучей, что позволяет легко определять алмазы среди сходных по внешнему облику минералов, а также отличать бриллианты от всевозможных подделок. А вот ультрафиолетовые лучи многие алмазы совершенно не пропускают.
Твердость является, как уже отмечалось, весьма важным свойством алмаза, определяющим его исключительно большую роль в производственной деятельности человека. Под твердостью обычно подразумевается сопротивление одного тела проникновению в него другого. Для качественного определения относительной твердости минералов широко используется так называемая шкала твердости (шкала Мооса), предложенная в начале XIX в. Шкала включает десять минералов-эталонов, расположенных в порядке возрастания твердости. При этом порядковые номера эталонов принимаются в качестве баллов твердости.
Минералогическая шкала твердости
| Минерал-эталон | Баллы твердости |
| Тальк - Mg3(OH)2[Si4O10] | 1 |
| Каменная соль - NaCl | 2 |
| Кальцит - CaCO3 | 3 |
| Флюорит (плавиковый шпат) - CaF2 | 4 |
| Апатит - Ca5F(PO4)3 | 5 |
| Ортоклаз (полевой шпат) - K[AlSi3O8] | 6 |
| Кварц - SiO2 | 7 |
| Топаз - Al2(F,OH)2[SiO4] | 8 |
| Корунд - Al2O3 | 9 |
| Алмаз - C | 10 |
Твердость веществ на основе шкалы Мооса определяют, с усилием проводя ребром или острым сколом изучаемого объекта по гладкой поверхности какого-либо эталонного минерала. Если вещество тверже взятого эталона, то на поверхности последнего остаются бороздки, царапины. При меньшей твердости изучаемого вещества относительно минерала-эталона оно не оставляет царапин на его поверхности. При равной твердости объекта и эталона неглубокие царапинки остаются на каждом из них. Алмаз, обладающий наивысшей твердостью, оставляет глубокие борозды на всех минералах и при этом сам не претерпевает ни малейших изменений.
Существуют и более точные, но вместе с тем и значительно более сложные способы определения твердости. Не останавливаясь на их описании, упомянем о двух наиболее широко применяемых. Один из них основан на учете скорости сошлифовки (обдирки) испытываемого вещества при стандартных условиях. Другой способ заключается в измерениях, выполняемых с помощью специального прибора - твердометра. Рабочим органом его служит четырехгранная (а для замеров на особо твердых телах трехгранная) алмазная пирамидка. Острие пирамидки под определенной нагрузкой вдавливают в полированную поверхность изучаемого объекта и по величине получающегося углубления вычисляют показатель твердости (микротвердость) вещества в килограмм-силах на квадратный миллиметр. Величина этого показателя составляет для талька 2,4, кальцита 109, апатита 536, кварца 1120, корунда 2060, алмаза 10060.
Твердость алмазов, как и других минералов, не остается постоянной на различных гранях одного и того же кристалла. Ювелиры давно заметили, что при шлифовке кристаллов алмаза наименьшее сопротивление оказывают грани куба, несколько большее - ромбододекаэдрические грани и наибольшее - грани октаэдра. Детальными исследованиями в наше время установлены ощутимые колебания твердости даже по различным направлениям в пределах единой грани кристалла.
Доказано, что твердость различных граней алмазных кристаллов находится в прямой зависимости от плотности расположения атомов углерода на плоскостях, соответствующих той или иной грани. Такие плоскости, включая не только поверхности граней, но и бесчисленное множество параллельных им плоскостей внутри кристалла, называются плоскими сетками. Количество атомов, приходящееся на единицу поверхности плоской сетки, принимается за ее плотность. Плотность октаэдрических, ромбододекаэдрических и кубических сеток в алмазе выражается отношением 2,308:1,414:1. В этой же последовательности, как уже отмечалось, убывает и твердость граней кристаллов.
Аналогичной закономерности подчиняется распределение твердости и по различным направлениям в пределах каждой отдельно взятой грани: относительно пониженной твердостью обладают те направления, которые характеризуются наибольшими расстояниями между атомами (рис. 15).
![Рис. 15. Направления наименьшей твердости (стрелки) на различных гранях природных кристаллов алмаза (по И. И. Шафрановскому) [11]. Буквами обозначены грани: о - октаэдра, д - ромбододекаэдра, к - куба](pic/000020.jpg)
Рис. 15. Направления наименьшей твердости (стрелки) на различных гранях природных кристаллов алмаза (по И. И. Шафрановскому) [11]. Буквами обозначены грани: о - октаэдра, д - ромбододекаэдра, к - куба
Широко известны существенные различия в средней твердости алмазов из разных месторождений. Основными причинами этого являются, по всей вероятности, наличие или отсутствие некоторых примесей в алмазах и изменчивость степени совершенства кристаллической решетки, которая в зависимости от физических и химических условий кристаллизации алмаза может иметь большее или меньшее число всевозможных дефектов.
Следует подчеркнуть, что даже самые "мягкие" алмазы во много раз превосходят по твердости корунд и все остальные минералы.
Наряду с исключительно высокой твердостью алмаз обладает свойством раскалываться под воздействием достаточно сильных и резких механических воздействий, ударов. При этом независимо от внешней формы алмазов они, как правило, раскалываются по плоскостям, параллельным граням октаэдра. Способность кристаллов колоться по определенным поверхностям, параллельным их граням, в минералогии называется спайностью. Поскольку октаэдр имеет восемь попарно параллельных граней, то, следовательно, спайность алмаза параллельна четырем плоскостям.
Спайность по плоскостям октаэдра у кристаллов алмаза обусловлена неравномерным расположением парных плоских атомных сеток, ориентированных параллельно граням октаэдра. Расстояние между двумя парами этих сеток почти втрое больше расстояния между сетками, образующими каждую пару. Спайность алмаза при его обработке позволяет вместо сошлифовки откалывать кусочки кристалла, обладающие дефектами или мешающие приданию необходимой формы бриллиантам и всевозможным техническим изделиям из алмаза (фильерам, резцам и др.).
Алмаз является хорошим проводником тепла. При трении он электризуется. Выше уже упоминалось, что некоторые алмазы обладают полупроводниковыми свойствами и относятся к полупроводникам р-типа. Энергия активации акцепторов у них составляет 0,35-0,40 эв, а удельное сопротивление в интервале температур от -100 до 600° С изменяется в пределах 250-750 ом*см.
Предполагается, что полупроводниковые свойства алмазов обусловлены наличием в них примеси бора.
Весьма важным и интересным свойством алмазов является также возникновение световых вспышек и импульса электрического тока при попадании в кристалл быстрых заряженных частиц. Световые вспышки (сцинтилляции) в алмазах настолько интенсивны, что любой источник ядерного излучения с энергией выше лишь нескольких тысяч электрон-вольт надежно регистрируется при использовании обычных фотоэлектронных умножителей.
Интенсивность сцинтилляции мало зависит от энергии электронов. Она почти постоянна при температуре ниже -50° С, но с повышением температуры убывает и исчезает полностью при 100° С. Какой-либо связи между сцинтилляционной способностью и другими свойствами алмаза пока не установлено. Исследования в интервале -125÷+ 230°С показали, что счетная способность и фотопроводимость алмаза увеличиваются с понижением температуры. Достоинствами алмазных счетчиков являются прочность, стабильность, долговечность даже в весьма агрессивных средах, а также в окружении сильных магнитных и гравитационных полей.
Алмаз не поддается воздействию самых сильных кислот (соляной, серной, азотной, плавиковой), даже доведенных до кипения. Не реагирует он и со щелочами. И лишь в расплавах едких щелочей, селитры или соды алмаз окисляется и сгорает.
Опыты по нагреванию алмаза, начатые в середине XVII в. во Флоренции, были продолжены в наше время. Установлено, что при нагреве на воздухе до 850-1000° С алмаз сгорает. В струе чистого кислорода он загорается при 720-800° С. Начав гореть при слабом красном калении, камень быстро раскаляется добела и горит голубым пламенем.
Нагревание при нормальном атмосферном давлении без доступа кислорода до температуры выше 1200-1500° С приводит к превращению алмаза в графит. Процесс этот довольно медленный, причем скорость превращения возрастает при повышении температуры. Графитизация начинается на вершинках и ребрах, распространяется на всю поверхность кристалла, а затем и на внутренние части его. В итоге вместо сверкающего кристалла алмаза получаем тусклый черный агрегат графита, имеющий форму исходного камня, но несколько большего объема (из-за различий в плотности алмаза и графита). Обратного перехода графита в алмаз в условиях атмосферного давления осуществить не удается ни путем нагрева или охлаждения, ни какими-либо другими способами.
Таким образом, при атмосферном давлении устойчивой модификацией углерода является графит, а алмаз в этих условиях представляет собой неустойчивую (метастабильную) модификацию данного вещества. Если так, то возникают два вполне естественных вопроса. Во-первых, почему алмаз переходит в графит только при сильном нагреве, а при обычной температуре не изменяется на протяжении тысяч и, как увидим в последующих главах, даже сотен миллионов лет? Во-вторых, при каких же условиях происходит кристаллизация углерода в форме алмаза?
Ответ на первый из поставленных вопросов дают результаты исследований физико-химических процессов образования горных
Штриховые участки границ экспериментального подтверждения не имеют.
пород и минералов. Установлено, что реакции полиморфного превращения (в отличие, например, от плавления) протекают с большим трудом и незначительной скоростью. Для начала перехода одной модификации в другую, более устойчивую, необходимо, чтобы составляющие кристалл частицы (атомы, ионы) обладали определенным количеством энергии, достаточным для преодоления "энергетического барьера" при перестройке кристаллической структуры. Чем ниже температура, тем меньше вероятность преодоления такого "барьера" и скорость превращения.
При низких температурах скорость превращения может стать равной нулю и тогда метастабильная модификация будет сохраняться неопределенно долго.
Малая скорость превращения характерна для случаев, когда полиморфные модификации сильно различаются по своему кристаллическому строению. Именно благодаря очень сильным различиям в структуре кристаллических решеток не происходит самопроизвольного превращения алмаза в графит при обычных температурах на земной поверхности.
Ответ на второй вопрос - об условии кристаллизации углерода в виде алмаза - был получен в итоге теоретических исследований, результаты которых полностью подтвердились экспериментальными проверками.
Советский ученый О. И. Лейпунский на базе теоретических предпосылок рассчитал, что для превращения графита в алмаз в твердой фазе необходимы давление около 60000 кгс/см2 и температура 1700-1800° С. Он указывал также на возможное образование алмаза и при несколько меньших давлениях, если использовать вещества, характеризующиеся относительно невысокой температурой плавления и достаточной растворимостью углерода. В качестве одного из таких веществ называлось железо.
Таблица 2. Сопоставление некоторых свойств алмаза и графита
| Свойства | Алмаз | Графит |
| Структура | Атомы углерода размещаются плотно и каждый из них прочно связан с четырьмя окружающими атомами | Слоистая, образованная параллельными слоями шестиугольной сетки; связь между слоями слабая |
| Твердость по шкале Мооса | 10 (наивысшая) | 1 (минимальная) |
| Плотность | 3,47-3,56 | 2,21-2,23 |
| Ударная вязкость | Хрупкий | Вязкий |
| Спайность | Средняя по четырем направлениям (плоскостям) | Весьма совершенная по одной плоскости |
| Окраска | Бесцветная, желтая, бурая, серая, реже черная, синяя и красная | Серо-стальная и черная |
| Блеск | Сильный (алмазный) | Металлический |
| Электропроводность | Слабая (полупроводник р-типа, при трении электризуется) | Хорошая |
| Химическая стойкость | Не поддается воздействию кислот при комнатной температуре и кипячении. Сгорает в расплавах щелочей. На воздухе сгорает при 850-1000° С, в струе кислорода - при 720-800° С. Без доступа воздуха при нагревании выше 1200° С переходит в графит | С кислотами не реагирует. Сгорает в расплавах щелочей. Плавится при 3850 ±50° С |
В конце 50-х-начале 60-х годов XX в. термодинамические расчеты стабильности алмаза и графита при различных давлениях и температурах проводились многими исследователями.
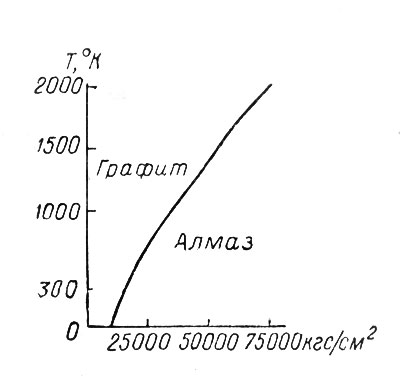
Рис. 16. Диаграмма равновесия графит-алмаз (по В. А. Николаеву и В. В. Доливо-Добровольскому)
Расчеты выполнялись с различными степенями приближения, но все они свидетельствуют о том, что образование алмаза возможно только при высоких давлениях, измеряемых десятками тысяч килограммов на квадратный сантиметр (рис. 16). Теоретические выводы о необходимости для образования алмаза высоких давлений полностью подтверждены экспериментально (рис. 17) и нашли широкое практическое применение. Заводы по изготовлению искусственных алмазов работают сейчас во многих странах мира, и общая продукция их исчисляется десятками миллионов карат. Подробнее эти вопросы рассматриваются в следующей главе.
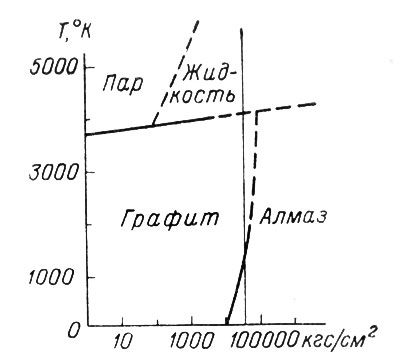
Рис. 17. Диаграмма состояния углерода при различных температурах и давлениях (по Бунди и др.)
Главнейшие различия между рассмотренными полиморфными модификациями углерода суммированы в табл. 2.
Недавно появились сообщения о том, что в Институте элементоорганических соединений Академии наук СССР получена новая, третья форма кристаллического углерода - карбин. В качестве исходного вещества при синтезе использовался ацетилен. Карбин, как и некоторые разновидности алмаза, обладает свойствами полупроводника и фотопроводимостью. Отмечалось присутствие близких к карбину форм кристаллического углерода в отдельных метеоритах.
Высокая химическая устойчивость и жаропрочность, сравнительно малая плотность, абсолютная немагнитность и многие другие свойства кристаллического углерода стимулируют поиски новых углеродных материалов. Весьма перспективным направлением таких исследований является синтез гибридных веществ, сочетающих отдельные свойства алмаза, графита и карбина. Первые шаги в этом направлении уже сделаны. Из каменного угля получено углеродное стекло, сочетающее жаропрочность и химическую устойчивость графита со свойствами полупроводника и обладающее еще меньшей плотностью. Поиски продолжаются.
|
ПОИСК:
|
© IZNEDR.RU, 2008-2020
При использовании материалов сайта активная ссылка обязательна:
http://iznedr.ru/ 'Из недр Земли'
При использовании материалов сайта активная ссылка обязательна:
http://iznedr.ru/ 'Из недр Земли'