
Причины своеобразия слюды
Жарко. Мы сидим на вершине гольца, обращенного к Витиму, протекающему где-то внизу. Здесь лес вырублен, и ветерок, идущий снизу от реки, сдувает всех комаров. Можно немного отдохнуть после длительного пути по выработкам, в тайге, где над каждым из нас клубилась черная туча комаров.
Под нами разведочная канава. Только что здесь взята проба: из выработки вынут тщательно замеренный объем породы, обычно это около 1-2 м3, и из нее выбрана вся слюда. Кучка слюды еще лежит рядом. В ближайшие дни эта кучка в строго маркированных ящиках будет отправлена на фабрику, где слюду очистят, выделят из нее все ценное, а отходы откинут, и можно будет точно сказать о содержании слюды в жиле, а может быть и о ее запасах. Это в будущем, но и сейчас уже видно, что жила богатая; кучка отобранной слюды довольно большая; слюда хорошая и легко расщепляется.
Мы - это очень серьезные люди; два профессора - один из Ленинграда, другой из Москвы, главный геолог районного Геологического управления, геолог рудника, геолог участка, проводящий здесь разведку, и два молодых студента, "бравших пробу": хорошенькая девчоночка и паренек с любопытными глазами, оба "вдребезги" искусанные комарами. Разговор наш тоже очень серьезен, рудник почти исчерпал разведанные ранее запасы слюды, через некоторое время некуда будет ставить рабочих. Разведку нужно срочно направить так, чтобы она по возможности скорее выявила бы слюдоносные жилы. Выработка, на которой мы сидим, позволяет надеяться на нужные результаты; но как зацепиться за эту выработку? Куда пойти дальше? И мы спорим, взвешивая все "за" и "против".
В разгаре спора мне вдруг становится не по себе: что же я делаю? Взял кусок слюды из лежащей рядом пробы и усиленно его разрываю на мелкие листочки. Чем активнее спор, тем быстрее движутся мои руки, и тем тоньше листочки, падающие на землю. Я ведь порчу пробу; из этого куска выйдет несколько граммов деловой слюды, правда, при общем содержании слюды во многие десятки килограммов эта потеря не так велика, но все же портить пробу совершенно недопустимо для геолога. Отрываюсь от спора, смотрю на моих спутников, и у каждого из них в руках по кусочку слюды, и каждый "дерет" слюду ничуть не меньше моего. Ленинградский профессор очень интересно, просто талантливо, рассказывает об особенностях рассматриваемой жилы, которые мы все видели, но никто ранее не придавал им значения, а вместе с тем именно они, эти особенности, решают всю проблему. Однако и у него в руках оторванный листочек слюды. Смотрю на геолога рудника, за ним последнее слово, он соглашается и вместе с тем не соглашается, "внимательно", явно ничего не видящим взглядом, смотрит на кусок слюды, который держит в руках, отрывает от него тонюсенький листочек и кладет на прежнее место; листочек немедленно приклеивается; геолог пытается оторвать его, ничего не получается, зацепляет ногтем, но слюда рвется по свежему месту. Бросает кусок, и, продолжая слушать, берет новый кристалл слюды и снова начинает его "щипать". Даже девчоночка, которая, открыв рот и смотря большими глазами на знаменитого профессора, внимательно его слушает, держит в руках кусочек слюды, от которого время от времени отрывает тонкие листочки и бросает на землю.
Наконец спор закончен; все единодушно решили, что жила "стоящая"; на основе немногих признаков наметили ее возможное продолжение и решили подсечь ее на глубине с помощью буровых скважин. Сейчас же геолог рудника отдал приказ, и уже на следующий день к жиле начали пробивать просеку для перевозки буровой установки. Забегая вперед, скажу, что жила оправдала наши ожидания и дала много хорошей слюды.
Описывая наш спор на вершине гольца, я совсем не имел в виду судьбу жилы. Меня заинтересовало другое; споря на месторождении все участники совершенно механически щипали слюду. Позднее я всегда стал присматриваться к людям, имеющим дело со слюдой, и должен отметить, что щипка слюды удивительно завлекательное занятие, и оно так же захватывающе, как "лузганье" семечек.
Способность слюды разрываться на тончайшие пластинки изумительна. Она присуща слюдяному кристаллу, и чем лучше кристалл, тем совершеннее эта способность. Прекрасно раскалываются как природные, так и синтетические кристаллы. Причина этой способности, безусловно, лежит в структуре слюдяных кристаллов.
Слюда принадлежит к группе минералов, которая носит название силикатов. В этом названии подчеркнуто, что основу химического состава слагает кремнезем - окись кремния (или силиция). Кислород и кремний определяют структуру всех силикатов. Мы уже имели случай упоминать, что кремний четырехвалентен и поэтому каждый атом кремния связан с четырьмя атомами кислорода. Каждый из двухвалентных атомов кислорода с атомом кремния связан одной связью, вторая же остается свободной и может войти в соединение с каким-либо другим катионом или другим атомом кремния.
Четыре атома кислорода расположены на равных удалениях один от другого, а это возможно только в том случае, если эти атомы расположены в углах правильного четырехгранника - тетраэдра, хорошо знакомого всем по форме молочных пакетов.
В структуре всех силикатов обязательно присутствуют такие кремне-кислородные тетраэдры, но роль их в структуре разных силикатов различна. Свободные кислородные связи тетраэдров могут быть связаны с каким-либо катионом, и тогда в составе минерала будет содержаться четыре атома кислорода на один атом кремния (SiO4). Такое строение имеют многие минералы, наиболее обычен среди них оливин, формула которого (Mg, Fe)2XSiO4 (К группе оливина относится чисто магнезиальный минерал форстерит Mg2SiO4, а к группе пироксена известково-магнезиальный диоксид MgCa(SiO3)2 - оба минерала очень широко распространены в районе слюдяных месторождений к югу от Иркутска). Однако возможны структуры, в которых один кислород связан с двумя кремниевыми нонами; такая связь может быть схематически изображена двумя тетраэдрами с одной общей вершиной. Возможны и более многочисленные связи между тетраэдрами, вплоть до того, что каждый кислород связан с двумя кремниями (рис. 38, б). Получается в результате сплошная вязь тетраэдров, как это имеет место у кварца, формула которого SiO2. Возможны и промежуточные случаи. Так, в структуре пироксена в каждом тетраэдре два атома кислорода являются общими с соседними (рис. 38, а), в результате возникает единая цепочка тетраэдров. В составе этих минералов на один кремний приходится два кислорода; формула наиболее простого минерала энстатита из группы пироксенов пишется как MgSiO3.
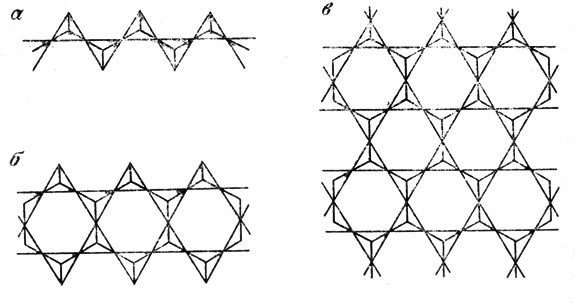
Рис. 38. Соединение кремне-кислородных тетраэдров через общий кислород. а - цепочка - основной элемент строения минералов группы пироксенов (диопсид); б - двойная цепочка ('пояс') - основной элемент строения минералов группы амфиболов; в - бесконечный лист - основной элемент строения слюд и других 'листовых силикатов'
В том случае, когда каждый кремне-кислородный тетраэдр связан общим кислородным атомом с тремя другими - возникает сплошная, в принципе, бесконечная сетка, в которой стороны тетраэдров образуют шестигранники, полностью выполняющие плоскость (рис. 38, в). Состав минералов с такой структурой изображается формулой, в которую обязательно входит частица Si4O10, именно это и имеет место у слюды. В разрезе (рис. 39) хорошо видно, что в сетке с одной стороны располагаются атомы кислорода, одна из валентностей которых свободна и может быть связана каким-либо катионом. В основе структуры слюды лежат две сетки, одна из которых располагается внизу, другая вверху, а выходящие в середину свободные кислороды насыщаются катионом, находящимся в промежутке. Промежуточным катионом обычно бывает алюминий (в мусковите) или магний (во флогопите). Такие очень прочные листочки в общей постройке слюды связаны между собой крупным одновалентным катионом, обычно калием.
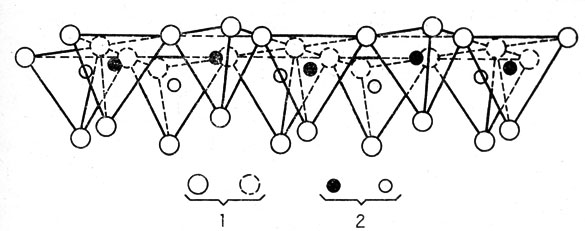
Рис. 39. Бесконечный лист кремне-кислородных тетраэдров. Вид сбоку; внизу располагаются 'свободные' кислородные ионы, обладающие способностью связывать катионы. 1 - ионы кислорода; 2 - ионы кремния
Уже простой взгляд на изображенную на рис. 40 структуру слюды, если, конечно, учесть, что она "бесконечно" продолжается во все стороны, позволяет видеть, что слюдяная постройка будет легко разрываться по плоскостям между структурными листочками (через калий) и будет очень трудно рваться поперек листов, что в действительности и имеет место. Структурой, близкой к структуре слюд, обладают и другие минералы (хлориты, тальк и др.), и все они очень легко разрываются на тонкие листочки; конечно, на свойствах таких, оторванных по спайности, листочков довольно сильно сказывается состав промежуточного слоя, характер межслоевой связи и расстояние между слоями. У слюд межслоевая связь слаба, а слои очень прочны, поэтому слюдяные кристаллы, если их раскалывать по спайности, дают тонкие и упругие листочки.
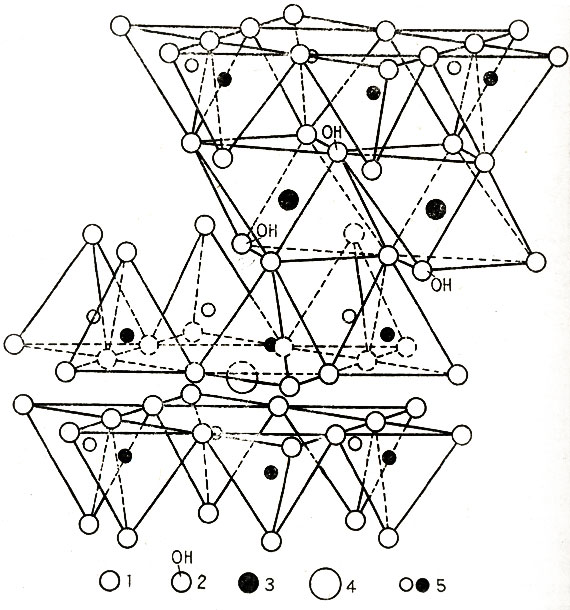
Рис. 40. Структура мусковита. Отчетливо видно, что основу слюды составляет трехслойный пакет, с обеих сторон которого располагаются листы кремне-кислородных тетраэдров. Направленные внутрь ионы кислорода этих листов насыщаются катионом, образующим третий внутренний слой (у мусковита этот катион представлен алюминием). Трехслойные пакеты связываются между собой через ион калия. 1 - кислород; 2 - гидроксил; 3 - алюминий; 4 - калий; 5 - кремний (на 1/4 замещен алюминием)
То, что разобранное только что строение слюды справедливо и что слюда действительно "рвется по калию", можно легко увидеть из очень простого опыта. Оторвите свежий листочек слюды и на место отрыва капните капельку раствора иодистого калия. Когда капля раствора высохнет, на поверхности слюды останутся мелкие кубические кристаллики иодистого калия. На слюде же, если посмотреть на кристаллики в лупу, все кристаллики выглядят как трехгранные пирамидки и все своими гранями ориентированы законно по отношению к слюде, хотя все они разные по размерам. Как будто кто-то разрезал кубики через углы и тщательно разложил параллельно один другому. Причина этого очень проста: расстояния между ионами калия на оторванном листочке слюды примерно такие же, как между ионами калия в кристалле иодистого калия. Поэтому в начале кристаллизации ион иода "ошибается" и садится на ионы калия, принадлежащие слюде, так же, как и на "свои" ионы. Таким образом, листочек слюды играет роль затравки для иодистого калия, а поскольку на всей поверхности листочка слюды ионы калия располагаются совершенно одинаково, постольку все кристаллы иодистого калия, нарастающие на эти ионы, тоже оказываются одинаково ориентированы.
При разрыве слюдяного кристалла часть ионов калия остается на нижней части листочка, часть на противоположной, верхней. Энергия, которую необходимо приложить для расщепления слюды, в конечном итоге идет именно на разрыв связей иона калия с обоими структурными слюдяными ионами. В свежеоторванных слюдяных листочках эти связи оказываются свободными, и если вскоре после отрыва на слюдяной листочек положить другой, тоже свежеоторванный, то может произойти весьма замечательное явление: оторванные листочки так плотно "приклеятся" друг к другу, что никакой возможности их вновь оторвать не будет, слюда будет рваться по новому месту. Особенно прочно такая "склейка" произойдет в том случае, если оба листочка будут находиться в параллельном положении или под углом около 60°. Тогда большое число свободных связей, разорванных при расщеплении, смогут в той или иной мере восстановиться.
Спайность - способность кристаллов раскалываться по определенным граням, очень строго связанным со структурой кристалла - замечательное и чрезвычайно важное свойство. У слюды эта способность выражена наиболее четко и лежит в основе ее использования.
При структурном единстве всех слюд химический состав отдельных их разновидностей резко различен, главным образом за счет выполнения промежуточного слоя. В наиболее распространенной группе промышленных слюд, в мусковитовых слюдах, в промежуточном слое располагается алюминий. Для них характерно большое постоянство состава, и, самое главное, в них, как правило, содержится очень мало железа. Вторая группа слюд, распространенная в природе значительно шире, чем мусковитовые слюды, характеризуется присутствием магния в промежуточном слое. Для этой группы слюд типично большое содержание железа; атом железа в структуре слюды может занимать то же место, которое занимал магний. В зависимости от состава эти слюды имеют и разные названия: чисто магнезиальные слюды и те слюды, в которых мало железа, называются флогопитами, а слюды, в которых железа примерно столько же, сколько и магния, называются биотитами, и наконец, почти чисто железистые - лепидомеланами. Флогопитовые слюды являются хорошими изоляторами и используются в промышленности, как и мусковит, а богатые железом биотитовые и лепидомелановые слюды имеют много худшую изоляционную способность, малопрозрачны, и поэтому не имеют практической ценности, хотя и встречаются в природе иногда в крупных листочках.
Различия в составе разных слюд определяют и условия их встречаемости в природе; мусковитовые слюды встречаются среди пород, богатых глиноземом, а флогопит можно найти только там, где вмещающие породы богаты магнием, но одновременно бедны железом, иначе возникнут слюды, богатые железом, но эти слюды, очень интересные для исследователя, не нужны промышленности.
|
ПОИСК:
|
© IZNEDR.RU, 2008-2020
При использовании материалов сайта активная ссылка обязательна:
http://iznedr.ru/ 'Из недр Земли'
При использовании материалов сайта активная ссылка обязательна:
http://iznedr.ru/ 'Из недр Земли'